 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
在870K和100kPa下,下列反应达到平衡
CO(g)+H2O(g)=CO2(g)+H2(g)
若将压力从100kPa提高到50000kPa,问:
(1)若各气体仍作为理想气体处理,其标准平衡常数有无变化?
(2)若各气体的逸度因子分别为γ(CO2)=1.09、γ(H2)=1.10、γ(CO)=1.23、γ(H2O(g))=0.77,则平衡应向何方移动?

 更多“在870K和100kPa下,下列反应达到平衡 CO(g)+H2O(g)CO2(g)+H2(g) 若将压力从100kPa提高到50000kPa,问: (1)”相关的问题
更多“在870K和100kPa下,下列反应达到平衡 CO(g)+H2O(g)CO2(g)+H2(g) 若将压力从100kPa提高到50000kPa,问: (1)”相关的问题
第1题
在870K和100kPa下,下列反应达到平衡

若将压力从100kPa提高到50000kPa,问:
(1)若各气体仍作为理想气体处理,其标准平衡常数有无变化?
(2)若各气体的逸度因子分别为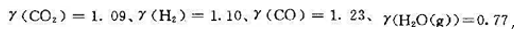 ,则平衡应向何方移动?
,则平衡应向何方移动?
第2题
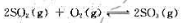
反应达到平衡时,测得混合物中有6.0molSO2(g)。试计算:
(1)该可逆反应在800K时的标准平衡常数和标准摩尔吉布斯自由能变;
(2)SO2在上述条件下的平衡转化率。
第4题
在298K、100kPa下,反应A(g) C(g)+2B(g)达到平衡时,A的平衡转化率为a1.在此条件下加入情性气体.A的平衡转化率为a2,,则a1()a2.若减压后,A的平衡转化率为a3,则a1()a3.(填>,<,=)
C(g)+2B(g)达到平衡时,A的平衡转化率为a1.在此条件下加入情性气体.A的平衡转化率为a2,,则a1()a2.若减压后,A的平衡转化率为a3,则a1()a3.(填>,<,=)
第5题
第6题
A.0.76
B.1.3
C.0.67
D.4.0
第7题
已知100kPa下,CaCO3(s)的分解温度为1155K.下列反应:CaCO4(s) CaO(s)+CO2(g)在800K和1155K之间.
CaO(s)+CO2(g)在800K和1155K之间.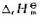 =177.9kJ·mol-1.则800K时反应的Kpθ=().
=177.9kJ·mol-1.则800K时反应的Kpθ=().
A.1
B.2.69X10-4
C.26.9
D.100
第8题
在600℃,100kPa时下列反应达到平衡:
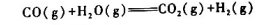
现在把压力提高到5×104kPa,问:
(1)若各气体均视为理想气体,平衡是否移动?
(2)若各气体的逸度因子分别为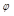 (CO2)=1.09,
(CO2)=1.09,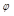 (H2)=1.10,
(H2)=1.10,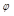 (CO)=1.20,
(CO)=1.20,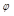 (H2O)=0.75,与理想气体反应相比,平衡向哪个方向移动?
(H2O)=0.75,与理想气体反应相比,平衡向哪个方向移动?
第9题
五氧化二磷(PCI3)分解反应
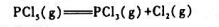
在200℃时的K°=0.312,计算:
(1)200℃,200kPa下PCI3的解离度;
(2)摩尔比为1:5的PCI3与CI2的混合物,在200℃,100kPa下达到平衡时PCI3的解高度.
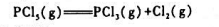
第10题
A.向生成NO2(g)的反向进行
B.正好达到平衡
C.难以判断其进行方向
D.向生成N2O4(g) 的方向进行
第11题
A.向生成NO2(g)的反向进行
B.正好达到平衡
C.难以判断其进行方向
D.向生成N2O4(g) 的方向进行

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
