 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
试设计一个电池,使其中进行下述反应:

(1)写出电池表示式;
(2)计算25℃时,上述电池反应的Kθ;
(3)若将过量的银粉加到浓度为0.05mol·kg-1的Fe(NO3)3溶液中,求反应达平衡后Ag+的浓度为多少?(设活度系数均为1).已知φθ(Fe3+|Fe2+)=0.771V,φθ(Ag|Ag+)=0.7991V.
 更多“试设计一个电池,使其中进行下述反应:(1)写出电池表示式;(2)计算25℃时,上述电池反应的Kθ”相关的问题
更多“试设计一个电池,使其中进行下述反应:(1)写出电池表示式;(2)计算25℃时,上述电池反应的Kθ”相关的问题
第2题
298K时,有反应Pb(s)+Cu2+(a=0.5)→Pb2+(a=0.1)+Cu(s),试为该反应设计电池,并计算:
(1)电池电动势;
(2)电池反应的Gibbs能变化;
(3)若将上述反应写成2Pb(s)+2Cu2+(a=0.5)→2Pb2+(a=0.1)+2Cu(s),(1)、(2)所得结果有何变化?
第3题
试为下述反应设计一电池
Cd(s)+I2(s)====Cd2+(a=1)+2I-(a=1)
求电池在298K时的标准电动势E、反应的△rG和平衡常数Kθ。
第4题
在25℃时,电池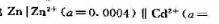 0.2)|Cd的标准
0.2)|Cd的标准
电动势Eθ=0.360V,试写出该电池的电极反应和电池反应,并计算其电动势E值.
第5题
电池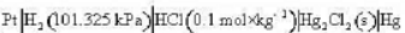 电动势召与温度T的关系为
电动势召与温度T的关系为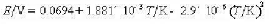
(1)写出电池反应:(2)计算25°C时该反应的DrCm.DrSm.DrHm以及电池恒温可逆放电时该反应过程的Qr.m
第6题
298K时,已知
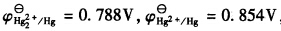 ,试计算:(1)反应Hg2++2e→
,试计算:(1)反应Hg2++2e→
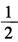 Hg22+的标准电极电势;(2)为反应Hg+Hg2+→Hg22+设计电池,并计算该反应的标准平衡常数。
Hg22+的标准电极电势;(2)为反应Hg+Hg2+→Hg22+设计电池,并计算该反应的标准平衡常数。
第7题
写出下列各电池的电池反应。应用表7.7.1(在教材中)的数据计算25℃时各电池的电动势及电池反应的摩尔吉布斯函数变,并指明各电池反应能否自发进行。
(1)Pt|H2(g,100kPa)|HCl[a(HCl)=1]|Cl2(g,100kPa)|Pt
(2)Zn|ZnCl2[a(ZnCl2)=0.5]|AgCl(S)|Ag
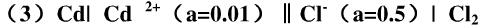
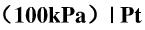
第8题
某湖水中含有Cl-并略带酸性,设计一个方便的电池,测定其中Cl-浓度。写出电池符号和被测半电池的电极电势表示式。
第9题
测得电池Zn|ZnCl2(a=0.05)|AgCl(s)|Ag的电动势在298.15K时为1.015V,温度系数TCR为-4.92×10-4V/K,试写出电池反应并计算当电池可逆放电2mol电子电量时,电池反应的△rGm、△rSm、△rHm及电池的可逆热Qr。
第10题
试设计3个原电池,使它们的电池反应均为
2Fe3++Fe=3Fe2+
并根据下面的元素电势图计算每个原电池的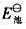 ,再计算电池反应的
,再计算电池反应的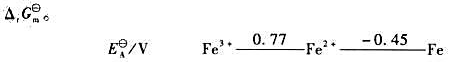

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
