 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
 更多“用钙离子选择性电极和SCE置于100mlCa2+试液中,测得电位为0.415V.加入2ml浓度为0.218mol·L-1的Ca2标准溶液后,测得电位为0.430V.计算Ca2+的浓度.”相关的问题
更多“用钙离子选择性电极和SCE置于100mlCa2+试液中,测得电位为0.415V.加入2ml浓度为0.218mol·L-1的Ca2标准溶液后,测得电位为0.430V.计算Ca2+的浓度.”相关的问题
第1题
用钙离子选择电极和饱和甘汞电极置于100mL Ca2+试液中,测得电动势为0.415V。加入2.00mL浓度为0.218mol·L-1Ca2+标准溶液后,测得电势为0.430V。计算Ca2+的浓度。
第2题
得电位值为+129.7mV(对SCE);另取水样10.00mL,加入离子强度调节缓冲剂25.00mL,再加入氟离子质量浓度为0.0100mg·mL-1的标准液5.00mL用水稀释至50.00mL,测得电位值为+98.2mV(对SCE)。氟电极的响应斜率为58.0mV/pF,求水样中F-的质量浓度。
第3题
25℃时,用钙离子选择性电极(负极)与饱和甘汞电极(正极)组成电池,在25.0mL试液中测得电动势为0.4965V,加入2.00mL 5.45×10-2mol·L-1Ca2+标准溶液后,测得电动势为0.4117V,试求试液的p(Ca2+)。
第4题
下列电池(25℃):
S2-选择性电极|S2-(a=1.00×10-3mol·L-1)||SCE
其电动势为0.315V。用未知硫离子S2-溶液代替上述已知浓度的S2-溶液,测得电动势为0.248V。试计算未知溶液中S2-浓度。(液接电位忽略不计)
第5题
第6题
用氯离子选择性电极测定果汁中氯化物含量时,在100mL果汁中测得电动势为-26.8mV,加入1.00mL浓度为0.500mol·L-1经酸化的NaCl溶液,测得电动势为-54.2mV。计算果汁中氯化物浓度。(假定加入NaCl前后离子强度不变)
第7题
用氟离子选择性电极与Ag/AgC1电极组成测量电池

取25.00mL水样加入25.00mL总离子强度调节液得溶液A,测得其电池电动势为-325mV,若在A溶液中加入1mL1.00X10-3mo1/L溶液,测得电池电动势为-31TmV,若将A溶液用总离子强度调节液稀释一倍,测得电动势为-342mV,求水样中含氟的浓度为多少?
第8题
用氟离子选择性电极测定牙膏中F-含量。称取0.2000g牙膏并加入50mL缓冲试剂,搅拌微沸冷却后移入100mL容量瓶中,用蒸馏水稀释至刻度。移取25.00mL于烧杯中测得其电位值为0.155V,加入0.10mL0.50mg·mL-1F标准溶液后,测得电位值为0.134V。该离子选择电极的斜率为59.0mV/pF。试计算牙膏中氟的质量分数。
第9题
在25℃时,用标准甘汞电极(SCE)作正极,Ca2+选择性电极作负极,放入 0.001mo1/L的Ca2+溶液中,测得电动势为-0.159V。换用含Ca2+的未知溶液后,测得电动势为-0.212V。问未知溶液的Ca2+浓度为多少?己知25℃时,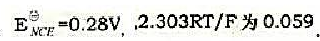
第10题
25℃时,下列电池的电动势为0.411V:
(—)镁离子电极|Mg2+(1.8×10-3mol·L-1)||饱和甘汞电极()
用含Mg2+试液代替已知浓度的溶液时,测得电池的电动势为0.439V,求试液中的pMg。
第11题

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
