 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
A.再沉淀
B.升高沉淀体系温度
C.增加陈化时间
D.减小沉淀的比表面积
 更多“A-B-304 4 2 3沉淀中若杂质含量太大,则应采取()措施使沉淀纯净”相关的问题
更多“A-B-304 4 2 3沉淀中若杂质含量太大,则应采取()措施使沉淀纯净”相关的问题
第1题
工业上利用铅浮渣(主要成分是PbO,Pb,含有少量Ag,CaO和其他不溶于硝酸的杂质)生产硫酸铅和硫化铅纳米粒子,流程如图所示: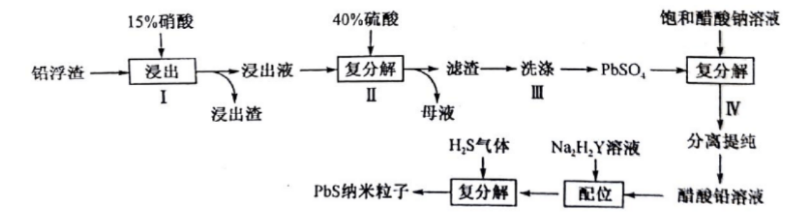 已知:25℃时,
已知:25℃时,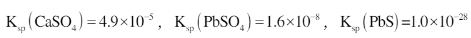 (1)步骤Ⅰ需控制硝酸的用量并使Pb稍有剩余,浸出渣的成分除了不溶于硝酸的杂质和铅外,还主要有()。
(1)步骤Ⅰ需控制硝酸的用量并使Pb稍有剩余,浸出渣的成分除了不溶于硝酸的杂质和铅外,还主要有()。
(2)写出Pb参加反应的化学方程式:()。保持铅剩余的原因是()。
(3)母液的主要成分是()(写化学式),可以循环利用。若母液中残留的SO42-过多,循环利用时可能出现的问题是()。
(4)若浸出液中c(Ca=2+)=0.05mol.L-1,步骤Ⅱ当pb2+完全沉淀后滤渣中是否有CaSO4存在?()(填有或没有)理由是()(通过计算说明)。
第2题
问题1、向含铜粉的稀硫酸中滴加浓硝酸,写出该反应的离子方程式()。问题2、制备流程中的A操作名称是()。如果铜粉、硫酸及硝酸都比较纯净,则制得的CuSO4•5H2O中可能存在的杂质是(),除去这种杂质的实验操作称为()问题3、如果采用重量法测定CuSO4-5HO的含量,完成下列步骤。①()②加水溶解③加氯化钡溶液,沉淀④过滤(其余步骤省略)。在过滤前,需要检验是否沉淀完全,其操作是()。如果1.040g提纯后的试样中含CuSO•5HO的准确值为1.015g,而实验测定结果是1.000g,测定的相对误差为()问题4、已知:CuSO4+2NaOH→Cu(OH)2↓:1+Na2SO4.称取0.1000g某CuSO4•5H2O试样(杂质不与氢氧化钠溶液反应)于锥形瓶中,加入0.1000mo1/L氢氧化钠溶清28.00mL反府完全后,过量的氢氧化钠用0.1000mo1/L盐酸滴定至格点,托用盐酸20.16mL则0.1000g该试样中含CuSO4•5H2O()g上述滴定中,滴定管在用蒸馏水洗净之后,注入盐酸之前,还需进行的操作是()在滴定中,准确读数应该是滴定管上蓝线()所对应的刻度。
第3题
A.3
B.4
C.5
D.6
第4题
第5题
(1)能否以氢氧化物形式直接沉淀出Fe(OH)2以达到提纯CuCl2的目的?
(2)为了除去杂质铁,常用H2O2使Fe2+氧化为Fe3+,再调整pH以沉淀出Fe(OH)。请在NH3·H2O、Na2CO3、ZnO、Cu0等化学品中选择一种合适的用以.调整溶液的pH,并说明理由。
(3)Fe(OH)3开始沉淀出时的pH为多少?
(4)Fe(OH)3沉淀完全时的pH为多少?
参考答案:

1、某化工厂用盐酸加热处理粗CuO的方法以制备CuCl2,在所得溶液中每100mL有0.0568gFe2+杂质,请回答:
(1)能否以氢氧化物形式直接沉淀出Fe(OH)2以达到提纯CuCl2的目的?
(2)为了除去杂质铁,常用H2O2使Fe2+氧化为Fe3+,再调整pH以沉淀出Fe(OH)。请在NH3·H2O、Na2CO3、ZnO、Cu0等化学品中选择一种合适的用以.调整溶液的pH,并说明理由。
(3)Fe(OH)3开始沉淀出时的pH为多少?
(4)Fe(OH)3沉淀完全时的pH为多少?
第11题
A.有较高的选择性
B.形成的沉淀易吸附无机杂质,难洗涤
C.形成沉淀的水溶性较小
D.形成沉淀的相对分子质量较大

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
