 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
请计算298K和标准压力下,如下反应的标准摩尔焓变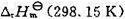 ,这个数值的1/4称为C-H键的“键焓"(平均值)。C(g) + 4H(g)=======CH4(g)
,这个数值的1/4称为C-H键的“键焓"(平均值)。C(g) + 4H(g)=======CH4(g)
已知:石墨升华为碳原子的焓变估计为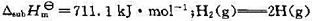 的标准解离焓
的标准解离焓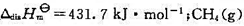 的标准摩尔生成焓
的标准摩尔生成焓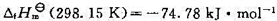 .
.
 更多“请计算298K和标准压力下,如下反应的标准摩尔焓变 ,这个数值的1/4称为C-H键的“键焓"(平均”相关的问题
更多“请计算298K和标准压力下,如下反应的标准摩尔焓变 ,这个数值的1/4称为C-H键的“键焓"(平均”相关的问题
第1题
反应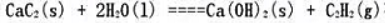 在298K下的标准摩尔热力学能变化量为-128kJ.mol-1。求该反应的标准摩尔焓变。
在298K下的标准摩尔热力学能变化量为-128kJ.mol-1。求该反应的标准摩尔焓变。
第2题
已知298K时,正辛烷C8H18(g)的标准摩尔燃烧焓为 -5512.4kJ.mol-1,二氧化碳CO2(g)和水H2O(1)的标准摩尔生成焓分别为393.5和-285.8mol-1;正辛烷C8H18(g)、氢气H2(g)和石墨C(s)的标准摩尔熵分别为463.71、130.68和5.74J.K-1.mol-1,计算 (1)298K时C8H18(g)生成反应的
1.jpg) (2)298K及标准压力下该生成反应达到平衡时C8H18(g)的摩尔分数; (3)讨论温度和压力对C8H18(g)生成反应的影响。
(2)298K及标准压力下该生成反应达到平衡时C8H18(g)的摩尔分数; (3)讨论温度和压力对C8H18(g)生成反应的影响。
第5题
已知下列反应的标准摩尔焓变,计算298K时SiC(s)的ΔH。
(1) C(s)+O2(g)====CO2(g),ΔH=-393.5 kJ·mol-
(2) Si(s)+CO2(g)====Si(s)+O2(g),△H=-989.2kJ/mol
第6题
已知下列反应在298K时的标准摩尔焓变:
已知下列反应在298k时的标准摩尔焓变
(1) 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(g)
(2) 2H2(g)+O2(g)=2H2O(l)
(3) C(石墨)+O2(g)=CO2(g)
(4) H2O(g)=H20(l)
根据以上数据 计算DfHmy(C2h2.g 298k )
第8题
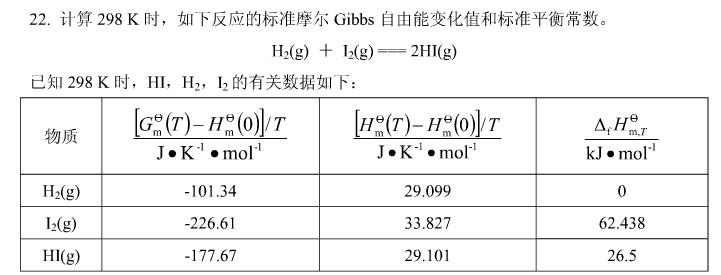
计算298K时,如下反应的标准摩尔Gibbs自由能变化值和标准平衡常数。
H2(g)+I2(g)====2HI(g)
已知298K时,HI、H2、I2的有关数据如下:
第9题
已知298.15K时下列反应的标准摩尔焓变
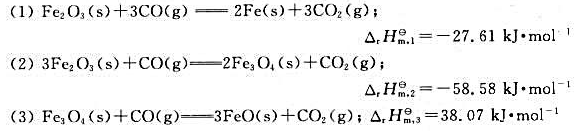
试计算下述反应在298.15K时的标准摩尔焓变
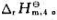
FeO(s)+CO(g)=Fe(s)+CO2(g)
第10题
用焓函数的数据计算合成氨反应:3H2+N2=2NH3的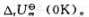 已知NH3的生成焓
已知NH3的生成焓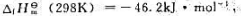 298K下N2、H2和NH3的焓函数
298K下N2、H2和NH3的焓函数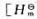
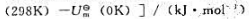 分别为8.67、8.47和9.92.
分别为8.67、8.47和9.92.
第11题
 Cp,m(H2,g)=29.07J·mol-1·K-1+(8.36×10-4J·mol-1·K-2)T
Cp,m(H2,g)=29.07J·mol-1·K-1+(8.36×10-4J·mol-1·K-2)T
Cp,m(O2,g)=36.16J·mol-1·K-1+(8.45×10-4J·mol-1·K-2)T
Cp,m(H2O,g)=30.00J·mol-1·K-1+(10.7×10-3J·mol-1·K-2)T
Cp,m(H2O,l)=75.26J·mol-1·K-1

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
