 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
从标准电极电势分析下列反应向哪一方向进行?
MnO2(s)+2Cl-(aq)+4H+(aq)→Mn2+(aq)+Cl2(g)+2H2O(l)
实验室往往利用该反应制备氯气,问应采取什么措施实现该反应?为什么?
 更多“从标准电极电势分析下列反应向哪一方向进行? MnO2(s)+2Cl-(aq)+4H+(aq)→Mn2+(aq)+Cl2(g)+2H2O(l) 实验”相关的问题
更多“从标准电极电势分析下列反应向哪一方向进行? MnO2(s)+2Cl-(aq)+4H+(aq)→Mn2+(aq)+Cl2(g)+2H2O(l) 实验”相关的问题
第1题
第2题
判断下列反应在标准态时进行的方向,如能正向进行,试计算反应进行的程度。已知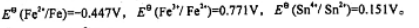
(1)Fe(s)+2Fe3+(aq)=3Fe2+(aq)
(2)Sn4+(aq)+2Fe2+(aq)=Sn2+(aq)+2Fe3+(aq)
分析:首先根据反应方程确定电池的正负极,即发生氧化反应的电对为负极,发生还原反应的为正极,然后根据正负极的电极电势的大小(若不是标准状态,则要根据能斯特方程计算出来)即电池的电动势的正负来判断反应的方向,并利用Kθ和标准电极电势的关系计算出反应进行的程度。
第3题
已知电极反应:
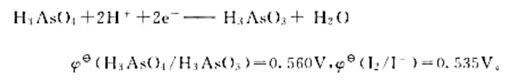
计算下列反应:
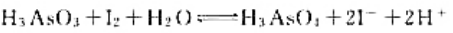
(1)在298K时的平衡常数;
(2)如果pH=7,其他物质浓度均为标准态,反应向什么方向进行?
(3)如果溶液的c(H+)=6.0mol·L-1.其他物质浓度均为标准态.反应向什么方向进行?
第5题
已知298.15K时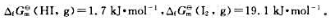 则化学反应
则化学反应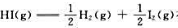 在298.15K时标准摩尔吉布斯自由能变
在298.15K时标准摩尔吉布斯自由能变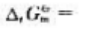 (),在标准状态下反应向方向自发进行。
(),在标准状态下反应向方向自发进行。
第6题
在标准状态下,下列两个反应均向正反应方向进行:
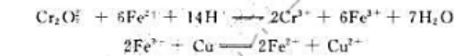
在上述三个电对中,标准电极电势最大的电对是(),标准电极电势最小的电对是()。
第7题
(1)计算298K下反应: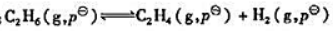 的
的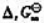 并判断在标准状态下反应向何方进行.
并判断在标准状态下反应向何方进行.
(2)计算298K反应: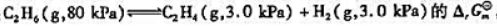 并判断反应方向.
并判断反应方向.
第8题
计算合成氨反应N2(g)+3H2(g)=2NH3(g)在673K时的标准平衡常数,并指出在673K,下列三种情况下反应向何方向进行? (1)P(NH3)=304kPa,P(N2)=171 kPa,P(H2)=2 022kPa; (2)p(NH3)=600kPa,P(N2)=625kPa,P(H2)=1 875kPa; (3)p(NH3)=100kPa,P(N2)=725kPa,P(H2)=2 175kPa。 在没有平衡浓度或平衡分压时,标准平衡常数KΘ 可由标准吉布斯函数变[△rGΘm]求得:△rGΘm(T)=-RTlnKΘ ,而 △rGΘm(T)≈△rHΘm(298K)-T△rSΘm(298K),所以,可根据热力学数据表中反应物和生成物的标准摩尔生成焓△rHΘm(298K)和标准摩 尔熵SΘm(298K)计算反应的标准焓变△rHΘm(298K)和标准熵变 △rSΘm(298K),进而计算出标准平衡常数KΘ。 气体反应在一定反应物和生成物分压下的方向,可由反应商J与平衡常数KΘ相对大小进行判断。
第10题
在1600℃时,反应[C]+[O]={CO},KC=416.67,问当真空度为1013.25Pa,[C]为0.05%,[O]为0.08%时,反应向哪一方向进行?

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
