 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
已知电极反应:
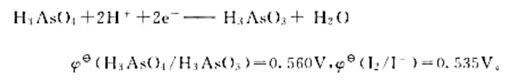
计算下列反应:
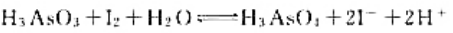
(1)在298K时的平衡常数;
(2)如果pH=7,其他物质浓度均为标准态,反应向什么方向进行?
(3)如果溶液的c(H+)=6.0mol·L-1.其他物质浓度均为标准态.反应向什么方向进行?
 更多“已知电极反应:计算下列反应:(1)在298K时的平衡常数;(2)如果pH=7,其他物质浓度均为标准态,反应”相关的问题
更多“已知电极反应:计算下列反应:(1)在298K时的平衡常数;(2)如果pH=7,其他物质浓度均为标准态,反应”相关的问题
第1题
已知下列电极反应的标准电极电势:
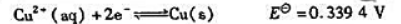
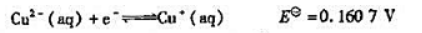
(1)计算反应: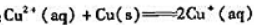 的KΘ;
的KΘ;
(2)已知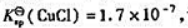 计算反应:
计算反应:
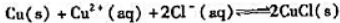 的标准平衡常数KΘ:
的标准平衡常数KΘ:
第3题
已知298.15K时, ,
, ,标准态时:(1)写出原电池符号(应自发进行);(2)写出电极反应及电池反应;(3)计算原电池的
,标准态时:(1)写出原电池符号(应自发进行);(2)写出电极反应及电池反应;(3)计算原电池的 ;(4)计算电池反应的
;(4)计算电池反应的 ;(5)求AgI的Ksp。
;(5)求AgI的Ksp。
第8题
A.Cl2+2e=2Cl-
B.2Cl--2e= Cl2
C.1/2 Cl2+e=Cl-
D.都是
第9题
298 K时,已知如下电池的标准电动势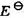 =0.2680V:
=0.2680V:
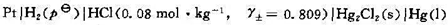
(1)写出电极反应和电池反应;(2)计算该电池的电动势;(3)计算甘汞电极的标准电极电势。
第10题
θ)|Pt
(1)写出电解时的电极反应及电解反应;
(2)计算298K时.在电流密度为50A·m-2条件下的分解电压.已知此时铂电极上的超电势:Eθ(OH,H2O|O2|Pt)=0.401V.η(H2)=0,η(O2)=0.487V;
(3)当所用的电流密度为50A·m-2时.计算使电解能顺利进行的最小分解电压.
已知ΔtGmθ(H2O,l)=-237.1kJ·mol-1.

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
