 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
A.12.48%
B.24.97%
C.30%
D.48%
 更多“已知溶液c(FeCl3)=1.9mol/L,密度ρ=1.234g/mL,则ω(FeCl3)是(),已知M(FeCl3)=162”相关的问题
更多“已知溶液c(FeCl3)=1.9mol/L,密度ρ=1.234g/mL,则ω(FeCl3)是(),已知M(FeCl3)=162”相关的问题
第1题
A、12.48%
B、24.97%
C、30%
D、48%
第2题
A.3Cl2+6FeI2===2FeCl3+4FeI3
B.Cl2+FeI2===FeCl2+I2
C.o2O3+6HCl===2CoCl2+Cl2↑+3H2O
D.2Fe3++2I-===2Fe2++I2
第3题
在10mL 0.08mol·L-1的FeCl3溶液中、加入含有0.1mol·L-1的NH3和1.0mol·L-1NH4Cl的混合溶液30mL,能否产生Fe(OH)4沉淀?(已知 (Fe(OH)3)=2.79×10-39)
(Fe(OH)3)=2.79×10-39)
第4题
已知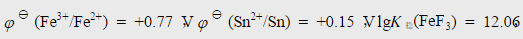 。通过计算说明下列氧化还原反应能否发生,若能发生写出其化学反应式。(设有关物质的浓度为1.0mol·dm-3)
。通过计算说明下列氧化还原反应能否发生,若能发生写出其化学反应式。(设有关物质的浓度为1.0mol·dm-3)
(1)向 溶液中加入SnCl2。
溶液中加入SnCl2。
(2)向FeCl3溶液中加入NaF,然后再加SnCl2。
第5题
称取Sb2S3试样1.2647g,将其在氧气流中灼烧所产生的SO2气体通入100mL FeCl3溶液中,使Fe3+还原至Fe2+,取该溶液10mL,用c(
第6题
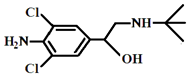
A.该物质的分子式为C12H17ON2Cl
B.该物质不溶于盐酸
C.该物质能与FeCl3溶液发生显色反应
D.该物质分子间都可以形成氢键
第7题
A.已知某FeCl3溶液中Fe3+的物质的量为1 mol,则Cl-的数目为3NA
B.标准状况下,22.4 L乙烷中所含共价键数目为6NA
C.100 g含氢元素质量分数为12%的乙烯和乙醛(C2H4O)的混合物中,所含氧原子数目为NA
D.在一定条件下,将0.1 mol N2和0.3 mol H2充分反应,转移的电子数目为0.6NA
第10题
A.班氏试剂、I2溶液和FeCl3溶液
B.FeCl3溶液、溴水和斐林试剂
C.溴水、托伦试剂和金属钠
D.NaOH溶液、I2溶液和FeCl3溶液

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
