 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
25℃时,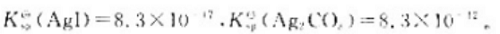 在25℃时用Na2CO3溶液处理AgI沉淀,能否使AgI沉淀转化为Ag2CO3沉淀?
在25℃时用Na2CO3溶液处理AgI沉淀,能否使AgI沉淀转化为Ag2CO3沉淀?
 更多“25℃时,在25℃时用Na2CO3溶液处理AgI沉淀,能否使AgI沉淀转化为Ag2CO3沉淀?”相关的问题
更多“25℃时,在25℃时用Na2CO3溶液处理AgI沉淀,能否使AgI沉淀转化为Ag2CO3沉淀?”相关的问题
第1题
用Na2CO3溶液处理AgI沉淀,使其转化为Ag2CO3沉淀。这一反应的平衡常数是多少?如果在1.0dm3Na2CO3溶液中要溶解0.010mol的AgI,则Na2CO3的最初浓度应为多少?这种转化能否实现?
第2题
25℃时,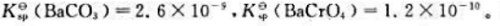 在25℃时将1.0gBaCO3沉淀转化为BaCrO4沉淀,至少需要将BaCO3沉淀溶解在多少毫升0.10mol·L-1K2CrO4溶液中?
在25℃时将1.0gBaCO3沉淀转化为BaCrO4沉淀,至少需要将BaCO3沉淀溶解在多少毫升0.10mol·L-1K2CrO4溶液中?
第3题
25℃时,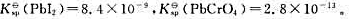 在含有PbI2沉淀的溶液中加入K2CrO4溶液,使其转化为PbCrO4沉淀,该沉淀转化反应的离子方程式为(),该沉淀转化反应的标准平衡常数
在含有PbI2沉淀的溶液中加入K2CrO4溶液,使其转化为PbCrO4沉淀,该沉淀转化反应的离子方程式为(),该沉淀转化反应的标准平衡常数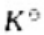 =()。
=()。
第4题
在25℃时,电池:
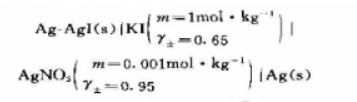
的电动势E=0.720V.试求:(1)AgI的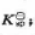 (2)AgI在纯水中的溶解度;(3)AgI在1mol·kg-1KI溶液中的溶解度.
(2)AgI在纯水中的溶解度;(3)AgI在1mol·kg-1KI溶液中的溶解度.
第5题
将3.0dm30.20mol·dm3K[Ag(CN)2]溶液和2.0dm30.30mol·dm-3KI溶液混合,是否会产生AgI沉淀?如欲不产生AgI沉淀,需先在K[Ag(CN)2]溶液中至少加入多少摩尔固体KCN(忽略体积变化)。已知K稳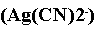 =1.3×1021,Ksp(AgI)=8.3×10-17。
=1.3×1021,Ksp(AgI)=8.3×10-17。
第6题
已知K(AgCl)=1.8X10-10,K(Ag2CO3)=8.45X10-12,K(AgI)=8.5x10-17,某溶液中含有浓度c均为0.10mol·L-1的Cl,CO32-、I-若向此溶液中滴加AgNO3溶液,产生沉淀的先后顺序是()。
A.AgI;Ag2CO3;AgCl
B.Ag2CO3、AgI;AgCl
C.AgCl ;Ag2CO3、AgI
D.AgI;AgCl;Ag2CO3
第7题
在PbSO4沉淀中加入K2CrO4溶液,发生下列沉淀转化反应:
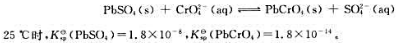
(1)计算25℃时该沉淀转化反应的标准平衡常数;
(2)若沉淀转化反应达到平衡时,SO42-的浓度为0.010mol·L-1,则溶液中CrO42-的浓度为多少?
第8题
第9题
第10题
25℃时,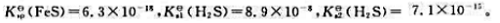 在0.10mol·L-1FeCl2溶液中通入H2S气体使之饱和,为了不生成FeS沉淀,溶液的pH应控制为多少?
在0.10mol·L-1FeCl2溶液中通入H2S气体使之饱和,为了不生成FeS沉淀,溶液的pH应控制为多少?
第11题
25℃时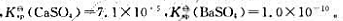 则沉淀转化反应:
则沉淀转化反应: 在25℃时的标准平衡常数
在25℃时的标准平衡常数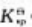 =()。在25℃标准状态下,上述反应方向为()。
=()。在25℃标准状态下,上述反应方向为()。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
