 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
请解释下列有关键长和键角的问题:
(1)在N3-离子中,两个N-N键由相等的键长,而在NH:中两个N-N键长却不相等;
(2)从NO+、NO到NO-的键长逐渐增大;
(3)NO2+、NO2、NO2-键角(∠ONO)依次为180°,134.39°、115.4°
(4)NH3、PH3、AsH3分子中的键角依次为107°、93.08°、 91.8°逐渐减小。
 更多“请解释下列有关键长和键角的问题:(1)在N3-离子中,两个N-N键由相等的键长,而在NH:中两”相关的问题
更多“请解释下列有关键长和键角的问题:(1)在N3-离子中,两个N-N键由相等的键长,而在NH:中两”相关的问题
第1题
第3题
已知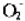 的键长为121pm,
的键长为121pm,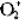 的键长为112pm,N,的键长为109pm,
的键长为112pm,N,的键长为109pm,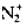 的键长为112pm,请予以解释,并预测
的键长为112pm,请予以解释,并预测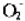 ,
,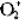 ,O2键长的顺序及N2,
,O2键长的顺序及N2,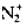 ,
, 键长的顺序.
键长的顺序.
第4题
已知OCl2分子中, CIOCl=110°,Cl-O键长为170pm;而在ClO2分子中,
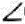 OCIO=115.5°,Cl-O键长为149pm.已知单键Cl-O键长为169pm,请用有关理论予以解释.
OCIO=115.5°,Cl-O键长为149pm.已知单键Cl-O键长为169pm,请用有关理论予以解释.
第7题
A.PCl 3 分子中三个P-Cl键的键长、键能、键角都相等
B.PCl 3 分子中P原子采取sp 3 杂化,其中三个用于形成P-Cl键,另一个为空轨道
C.PCl 3 分子中的P原子的价层电子对数为3,孤电子对数为1
D.PCl 3 是由极性键构成的非极性分子

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
