 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
 更多“298.15K时,将0.10molAgNO3固体溶于1.0L1.00mol·L-1NH3溶液中。 (1)若再溶入0.010molNaCl固体时,有无AgCl沉淀生成? (2)如果用NaBr固体代替Na…”相关的问题
更多“298.15K时,将0.10molAgNO3固体溶于1.0L1.00mol·L-1NH3溶液中。 (1)若再溶入0.010molNaCl固体时,有无AgCl沉淀生成? (2)如果用NaBr固体代替Na…”相关的问题
第1题
某固体混合物中可能含有KI,SnCl2,CuSO4,ZnSO4,FeCl3,CoCl2和NiSO4。通过下列实验判断哪些物质肯定存在,哪些物质肯定不存在,并分析原因。
(1) 取少许固体溶入稀硫酸中,没有沉淀生成。
(2) 将盐的水溶液与过量氨水作用,有灰绿色沉淀生成,溶液为蓝色。
(3) 将盐的水溶液与KSCN作用,无明显变化。再加入戊醇,也无明显变化。
(4) 向盐的水溶液中加入过量NaOH溶液有沉淀生成,溶液无明显颜色。过滤后,向溶液缓慢滴加盐酸时,有白色沉淀生成。
(5) 向盐的溶液中滴加AgNO3溶液时,得到不溶于硝酸的白色沉淀。沉淀溶于氨水。
第3题
应),得无色溶液C。将AgNO3溶液加入溶液C,析出白色沉淀D。D溶于氨水得溶液E,酸化溶液E,又产生白色沉淀D。将H2S通人溶液C,产生棕色沉淀F。F溶于(NH4)2S2形成溶液G。酸化溶液C,得黄色沉淀H。少量溶液C加人HgCl2溶液得白色沉淀I,继续:
加入溶液C,沉淀I逐渐变为灰色,最后变成黑色沉淀J。试确定各代号所示物质。
第4题
加入溶液(C),析出白色沉淀(D),(D)溶于氨水得溶液(E)。向(E)中加入KI,生成浅黄色沉淀(F),再加入NaCN时沉淀(F)溶解。酸化溶液(E),又产生白色沉淀(D)。将H2S通入溶液(C),产生灰色沉淀(G)。(G)溶于Na2S2,形成溶液。酸化该溶液时得一黄色沉淀(H)。少量溶液(C)加入HgCl2溶液得白色沉淀(J),继续加入溶液(C),沉淀(I)逐渐变灰,最后变为黑色沉淀(J)。试给出(A),(B),(C),(D),(E),(F),(G),(H),(I)和(J)所代表的物质的化学式,并用化学反应方程式表示各过程。
第5题
第6题
在298K和大气压力下,溶质NaCl(s)(B)溶于1.0kgH2O(l)(A)中,所得溶液的体积V与溶入NaCl(s)(B)的物质的量nB之间的关系为
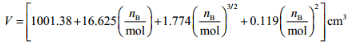 试求:(1)H2O(l)和NaCl的偏摩尔体积与溶入NaCl(s)的物质的量nB之间的关系;(2)nB=0.5mol时H2O(l)和NaCl的偏摩尔体积;(3)无限稀释时H2O(l)和NaCl的偏摩尔体积。
试求:(1)H2O(l)和NaCl的偏摩尔体积与溶入NaCl(s)的物质的量nB之间的关系;(2)nB=0.5mol时H2O(l)和NaCl的偏摩尔体积;(3)无限稀释时H2O(l)和NaCl的偏摩尔体积。
第7题
在100 mL 0.10 mol·L-1氨水中溶入1.07 g NH4Cl(s),则溶液的pH=_________,在此溶液中再加入100 mL水后,溶液的pH值将___________。[Kb(NH3·H2O)=1.8×10-5,NH4Cl相对分子质量为53.5]
第8题
某绿色固体A可溶于水,水溶液中通入CO2即得棕褐色固体B和紫红色溶液C。B与浓HCl溶液共热时得黄绿色气体D和近乎无色溶液E。将此溶液和溶液C混合即得沉淀B。将气体D通入A的溶液可得C。试判断A,B,C,D,E各为何物?写出各步反应方程式。
第9题
试根据上述实验现象判断各字母所代表的物质,并写出相关的反应方程式。
第10题
完成下列各反应的化学方程式: (1)Na2O2与过量冷水作用; (2)几滴热水滴在Na2O2固体上; (3)电解硫酸和硫酸铵的混合溶液; (4)将难溶于水和酸的Al2O3变成可溶于水的硫酸盐; (5)无氧条件下Zn粉还原酸式亚硫酸钠溶液; (6)将SeO2溶于水,然后通SO2气体; (7)用盐酸酸化多硫化铵溶液; (8)向硫代硫酸钠溶液中滴加少量硝酸银溶液; (9)向硝酸银溶液中滴加少量硫代硫酸钠溶液; (10)在中等酸度的钛(Ⅳ)盐溶液中加入H2O2。
第11题
将40.0ml 0.20mol/L NH3·H2O与20.0mL0.20mol/L HCl混合,所得溶液的pH为多少?若往此溶液中加入134.5mg固体CuCl2是否能生成沉淀?(假定加入固体后溶液体积不变)

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
