 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
 更多“已知某反应的活化能Ea=80kJ·mol-1,试求:(1)由20℃变到30℃;(2)由100℃变到110℃,其速率常数增大了多少倍?”相关的问题
更多“已知某反应的活化能Ea=80kJ·mol-1,试求:(1)由20℃变到30℃;(2)由100℃变到110℃,其速率常数增大了多少倍?”相关的问题
第1题
已知某气相反应的活化能Ea=163kJ·mol-1,温度390K时的速率常数k=2.37×10-2dm3·mol-1·s-1。试求温度为420K时的反应速率常数。
第2题
A.10
B.100
C.0.01
D.1
第3题
某反应A→Y,其速率常数kA=6.93min-1,则该反应物A的浓度从0.1mol·dm-3变到0.05mol·dm-3所需时间是( )。
A.0.2min B.0.1min
C.1min
第4题
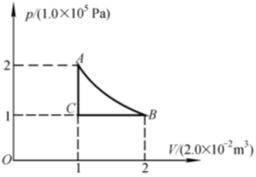
如图所示,使1mol氧气(1)由A等温地变到B;(2)由A等体地变到C,再由C等压地变到B.试分别计算氧气所作的功和吸收的热量.
第5题
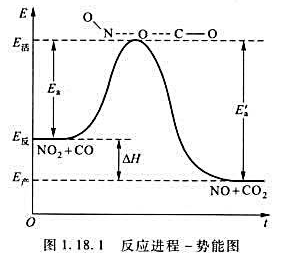
某基元反应:A→B其活化能Ea=60.4kg·mol-1,逆反应的活化能E'a=95.6kg·mol-1,
(1)试结合图1.18.1所示的反应进程-势能图,定性判断该反应是吸热反应,还是放热反应,求算该反应的ΔtH;
(2)若298K时的速率常数k=2.3×10-2s-1。试求373K时的速率常数;
(3)求算阿伦尼乌斯公式中的指前因子A。
第6题
A.反应速率常数由大到小变化
B.反应速率常数不变
C.反应级数由二级变为一级
D.反应级数由一级变为二级, k 由小变到大
第9题
CO(CH2COOH)2在水溶液中发生分解反应。已知60℃和10℃下的速率常数分别为5.48×10-2s-1和1.08×10-4s-1。(1) 求该反应的活化能:(2) 求反应在30℃下进行1000s时CO(CH2COOH)2的转化率。
第10题
已知某反应的活化能为70kJ·mol-1,300K时的速率常数为0.1s-1,试计算
(1)400K时,反应的速率为原来的多少倍?
(2)温度由1000K升高到1100K时,反应速率为1000K时的多少倍?
第11题
已知各基元反应的活化能如下表。
序号 | A | B | C | D | E |
正反应的活化能/(kJ·mol-1) | 70 | 16 | 40 | 20 | 20 |
逆反应的活化能/(kJ·mol-1) | 20 | 35 | 45 | 80 | 30 |
在相同的温度时:
(1) 正反应是吸热反应的是______;
(2) 放热最多的反应是______;
(3) 正反应速率常数最大的反应是______;
(4) 反应可逆程度最大的反应是______;
(5) 正反应的速率常数k随温度变化最大的是______。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
