 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
已知某反应的活化能为70kJ·mol-1,300K时的速率常数为0.1s-1,试计算
(1)400K时,反应的速率为原来的多少倍?
(2)温度由1000K升高到1100K时,反应速率为1000K时的多少倍?
 更多“已知某反应的活化能为70kJ·mol-1,300K时的速率常数为0.1s-1,试计算(1)400K时,反应”相关的问题
更多“已知某反应的活化能为70kJ·mol-1,300K时的速率常数为0.1s-1,试计算(1)400K时,反应”相关的问题
第1题
已知某反应在700K时,速率常数为:k=1.2dm3·mol-1·s-1,此反应的活化能为150kJ·mol-1,试计算800K时的反应速率常数。
第3题
第5题
某反应正反应的活化能为153kJ·mol-1,逆反应的活化能为80.6kJ·mol-1,则该反应的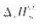 为()。
为()。
第8题
A.51.2kJ·mol-1
B. 345.7kJ·mol-1
C. 22.24kJ·mol-1
D. 150.1kJ·mol-1
第9题
A.81.06kJ•mol-1
B.2.145kJ•mol-1
C.162.1kJ•mol-1
D.4.291kJ•mol-1
第10题
A.201.3
B.-113
C.-201.3
D.113

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
