 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
某人计算M(OH)3沉淀在水中的溶解度时,不分析情况,即用公式Ksp=[M3+][OH-]3计算,已知Ksp=1×10-32,求得溶解度
某人计算M(OH)3沉淀在水中的溶解度时,不分析情况,即用公式Ksp=[M3+][OH-]3计算,已知Ksp=1×10-32,求得溶解度为4.4×1-9mol/L。试问这种计算方法有无错误?为什么?
 更多“ksp计算公式”相关的问题
更多“ksp计算公式”相关的问题
第2题
计算CaC2O4(1)在纯水中的溶解度;(2)在0.01mol/L(NH4)2C2O4溶液中的溶解度。已知CaC2O4的Ksp=2.3×10-9。
第3题
已知[Ag(NH3)2]+的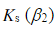 =1.6×107,AgI的Ksp=1.5×10-16。请计算AgI在2.0mol·L-1氨水中的溶解度。
=1.6×107,AgI的Ksp=1.5×10-16。请计算AgI在2.0mol·L-1氨水中的溶解度。
第4题
计算25℃时,Ag2CrO4在0.001mol.L—1AgNO3溶液中的溶解度(用mol.L—1表示)。[已知KspΘ)(Ag2CrO4)=1.1×10—12]
第5题
计算BaSO4在2.0mol/LHCl溶液中的溶解度。已知BaSO4的Ksp=1.1×10-10,H2SO4的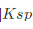 =1.2×10-2。
=1.2×10-2。
第6题
计算pH=3.0时CaC2O4的溶解度。(已知CaC2O4的Ksp=4.0×10-9,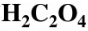 =5.9×10-2,
=5.9×10-2,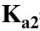 =6.4×10-5)
=6.4×10-5)
第7题
已知H2SO4的 =1.0×10-2,求PbSO4沉淀在0.10mol·L-1的HNO3中的溶解度。(Ksp=1.6×10-8)
=1.0×10-2,求PbSO4沉淀在0.10mol·L-1的HNO3中的溶解度。(Ksp=1.6×10-8)
第8题
比较AgCl在6mol·L-1氨水和水中的溶解度。已知KSP(AgCl)=1.8×10-10,KSP{[Ag(NH3)2]+}=1.12×107。
第9题
298K时,AgCl的Ksp=1.56×10-10,计算其在0.01mol/kgKNO3水溶液中的溶解度。
第10题
已知0℃,101.325kPa时,O2在水中的溶解度为4.49cm3/100g;N2在水中的溶解度为2.35cm3/100g。试计算被101.325kPa,体积分数ψ(N2)=79%,ψ(O2)=21%的空气所饱和了的水的凝固点较纯水的降低了多少?

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
