 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
比较AgCl在6mol·L-1氨水和水中的溶解度。已知KSP(AgCl)=1.8×10-10,KSP{[Ag(NH3)2]+}=1.12×107。
 更多“比较AgCl在6mol·L-1氨水和水中的溶解度。已知(AgCl)=1.8×10-10,{[Ag(NH3)2]+}=1.12×107。”相关的问题
更多“比较AgCl在6mol·L-1氨水和水中的溶解度。已知(AgCl)=1.8×10-10,{[Ag(NH3)2]+}=1.12×107。”相关的问题
第1题
将0.015mol氯化银沉淀置于500mL氨水中,若氨水平衡时的浓度为0.50mol·L-1,计算溶液中游离的Ag+浓度。(已知Ag+与NH3配合物的lgβ1=3.24,lgβ2=7.05,AgCl的Ksp=1.8×10-10)
第2题
第3题
已知
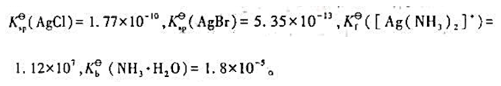
第4题
25℃时NaCl在水中的溶解度约为6mol·L-1,若在1L水中加入1mol的NaCl,则NaCl(s)+H2O(l)→NaCl(aq)的( )。
(A) △S>0, △G>0 (B) △S>0, △G<0
(C) △G>0, △S<0 (D) △G<0, △S<0
第6题
A.ΔS>0,ΔG<0
B.△S>0,△G>0
C.ΔS<0,ΔG>0
D.ΔS<0,ΔG<0
第7题
在0.1mol·L-1[Ag(NH3)2]+溶液中加入NaCl,使NaCl的浓度达到0.001mol·L-1时,问(1)有无AgCl沉淀出现?(2)在含有2mol·L-1氨水的0.1mol·L-1的[Ag(NH3)2]+溶液中加入NaCI,也使NaCl的浓度达到0.001mol·L-1时,问有无AgCl沉淀出现?(3)从两种情况中试得出必要的结论。
第9题

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
