 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
甲酸在金表面上的分解反应在温度为140℃和185℃时的速率常数分别为5.5×10-4s-1及9.2×10-2s-1,试求该反应的活化能。
 更多“甲酸在金表面上的分解反应在温度为140℃和185℃时的速率常数分别为5.5×10-4s-1及9.2×10-2s-1,试求该反应的活”相关的问题
更多“甲酸在金表面上的分解反应在温度为140℃和185℃时的速率常数分别为5.5×10-4s-1及9.2×10-2s-1,试求该反应的活”相关的问题
第2题
A.升高温度,分解反应的平衡常数减小
B.该反应是放热反应
C.该反应的焓变为正值
D.该反应是吸热反应
E.该反应的焓变为负值
第3题
第4题
反应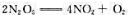 在某温度时速率系数为2.31×10-3s-1,计算:
在某温度时速率系数为2.31×10-3s-1,计算:
(1)反应进行了10min后,N2O5分解的百分率;
(2)N2O,分解反应的半衰期。
第5题
N2O5分解反应N2O5→2NO2+1/2O2是一级反应,已知其在某温度下的速率常数为4.8×10-4s-1。(1)求t1/2;(2)若反应在密闭容器中进行,反应开始时容器中只充有N2O5,其压力为66.66kPa,求反应开始后10秒和10分钟时的压力。
第6题
已知在高温下CO2按下式分解2CO2(g)→2CO(g)+O2(g),在压力为101.325kPa下,CO2的解离度在1000K和1400K时分别为2.50×10-5和1.27×10-2。若在1000K到1400K的温度区间内
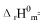 及1000K时的
及1000K时的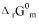 和
和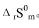 。
。
第7题
在600K时,某化合物分解反应的速率常数k=3.3×10-2s-1,反应的活化能Ea=18.88×104J·mol-1,若控制反应在10min内转化率达90%,则反应的温度应控制为多少?
第8题
第9题
第10题
已知下列热力学数据(T=298K)
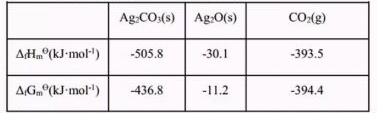
计算说明,要使Ag2CO3(s)=Ag2O(s)+CO2(g)分解反应在大气环境下(大气中CO2分压为30Pa)能自发进行,温度必须高于多少?

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
