 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
A.元素T是非金属元素
B.元素X是金属元素
C.元素T的原子半径比元素X小
D.元素X有2层电子
 更多“现有部分短周期元素的性质或原子结构如下表:元素编号元素性质或原子结构21世纪教育网TM层上的电子数是原子核外电子层数的2倍X最外层电子数是次外层电子数的2倍下列有关说法中正确的是()。”相关的问题
更多“现有部分短周期元素的性质或原子结构如下表:元素编号元素性质或原子结构21世纪教育网TM层上的电子数是原子核外电子层数的2倍X最外层电子数是次外层电子数的2倍下列有关说法中正确的是()。”相关的问题
第1题
第3题
第4题
下表是某些短周期元素的电负性(用x表示)的数值:
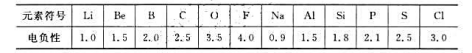
(1)通过分析上表中电负性的数值变化的规律,试确定Mg和N元素的电负性的数值范围() < x(Mg) < ()和() < x(N )< ()。
(2)同周期(同主族)元素的电负性与原子半径的关系是()。
(3)当形成化学键的两种元素的电负性的差值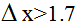 时,一般为离子键;当
时,一般为离子键;当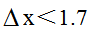 时,一般为共价键。则由此可知AlBr3中化学键的类型是()。
时,一般为共价键。则由此可知AlBr3中化学键的类型是()。
第6题
【题目描述】
第 2 题元素周期表是学习化学的重要工具。下面是元素周期表中1~18号元素原子核外电子排
布,我们对它进行研究:
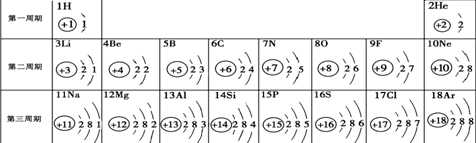
⑴ 第16号元素属于_______元素(填“金属”或“非金属”),它在化学反应中容易________(填“得”或“失”)电子;
⑵ 元素的化学性质与原子结构中的______________数关系密切;
⑶ 在同一族中,各元素的原子结构呈现的规律有________________ (任写一点);
⑷ 研究表明:第二周期从3~9号元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力逐渐增大,故原子半径逐渐减小。我分析第三周期从11~17号元素原子半径变化规律是 _________________________________。
【我提交的答案】:非金属 得 最外层电子数
【参考答案分析】:
⑴ 非金属 ;得 ;
⑵ 最外层电子 ;
⑶ 电子层数递增或最外层电子数相等或从上到下核电荷数增大等(只要合理均可)⑷ 逐渐减小
【我的疑问】(如下,请求专家帮助解答)
在同一族中,各元素的原子结构呈现的规律有________________ (任写一点);
⑷ 研究表明:第二周期从3~9号元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力逐渐增大,故原子半径逐渐减小。我分析第三周期从11~17号元素原子半径变化规律是 _________________________________。
第7题
分析:在本题的假设下,原有原子结构理论的有关规律的实质是有用的,但具体的则要发生一些变化。若泡利不相容原理和洪德规则就不适用;但能量最低原理是适用的;饱和的概念仍然成立,只是各个轨道、各个亚层、各个电子层最多能容纳的电子数应为原来的一半,如第二层排成2S2P3就饱和了,第三层排成3s13p33d5就饱和了;轨遭的能级顺序没有变化,电子的填充顺序也无变化。
第9题
第10题

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
