 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
向1.0L0.1mol·L-1[Ag(NH3)2]+溶液中加入KBr固体,当Br-浓度达0.1mol·L-1时,通过计算说明能否生成AgBr沉淀,能否通过改变氨水浓度来阻止AgBr沉淀生成。


 ,有AgBr析出。
,有AgBr析出。

 更多“向1.0L0.1mol·L-1[Ag(NH3)2]+溶液中加入KBr固体,当Br-浓度达0.1mol·L-1时,通过计算说明能否生成AgBr沉淀,能”相关的问题
更多“向1.0L0.1mol·L-1[Ag(NH3)2]+溶液中加入KBr固体,当Br-浓度达0.1mol·L-1时,通过计算说明能否生成AgBr沉淀,能”相关的问题
第1题
向1.0L0.1mol·L-1[Ag(NH3)2]+溶液中加入KBr固体,当Br-浓度达0.1mol·L-1时,通过计算说明能否生成AgBr沉淀,能否通过改变氨水浓度来阻止AgBr沉淀生成。
第2题
的影响)?
参考答案:
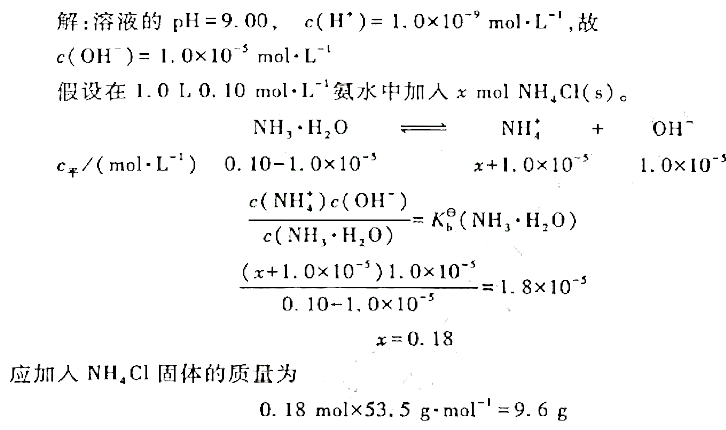
1、在1.0L0.1mol·L-1氨水中,应加入多少克NH4CI固体才能使溶液的pH=9.00(忽略固体的加入对溶液体积的影响)?
第3题
A.NH3·H2O的解离常数增大
B.NH3·H2O解离度增大
C.溶液的pH值增大
D.溶液的pH值降低
第5题
第6题
在0.01mol·L-1[Ag(NH3)2]+溶液中,含有过量的0.01mol·L-1氨水,计算溶液中的Ag+浓度。已知Kf([Ag(NH3)2]+)=1.6×107。
第7题
K[Ag(CN)2-]=1.0X1021,K[Ag(NH3)]2+=-1.6X107.
第8题
已知下列电池Zn|Zn2+(x mol·L-1)||Ag+(0.10mol·L-1)|Ag的电动势E=1.51V,求Zn2+的浓度。
第9题
计算25℃时,下列电池的电动势,并标明电池的正负极。
已知:E(AgCl/Ag)=0.222V,φSCE=0.245V
Ag,AgCl|NaCl(0.1mol·L-1),NaF(0.001mol·L-1)|LaF3单晶膜|NaF(0.1nol·L-1)‖SCE
第10题
A.0.2827 mol·L-1
B.0.7187 mol·L-1
C.0.043 mol·L-1
D.0.0100 mol·L-1
第11题
A.EcellӨ≠ 0,Ecell= 0
B.EcellӨ= 0,Ecell= 0
C.EcellӨ= 0,Ecell≠ 0
D.EcellӨ≠ 0,Ecell≠ 0

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
