 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
A.1-3x
B.1-2x
C.1-x
D.无法计算
 更多“已知由CuS、CuSO3、CuSO4组成的混合物中,硫元素的质量分数为x,则混合物中氧元素的质量分数为()”相关的问题
更多“已知由CuS、CuSO3、CuSO4组成的混合物中,硫元素的质量分数为x,则混合物中氧元素的质量分数为()”相关的问题
第1题
A.已知Fe与S能直接化合生成FeS,推测Cu与S可直接化合生成CuS
B.已知CaCO3与稀硝酸反应生成CO2,推测CaSO3与稀硝酸反应生成SO2
C.已知Na与水反应生成NaOH,推测Fe与水蒸气反应生成Fe(OH)3
D.已知Fe与CuSO4溶液反应,推测Fe与AgNO3溶液也能反应
第6题
有如下两个反应在323K时达成平衡:
(1)2NaHCO3(s)===Na2CO3(s)+H2O(g)+CO2(g)
(2)CuSO4·5H2O(s)===CuSO4·3H2O(s)+2H2O(g)
已知反应(1)的解离压力为4.0kPa,反应(2)的水气压力为6.05kPa。试计算由NaHCO3(s)、Na2CO3(s)、CuSO4·5H2O(s)和CuSO4·3H2O(s)所组成的系统,在达到同时平衡时CO2(g)的分压。
第7题
某地有软锰矿和闪锌矿两座矿山,它们的组成如下:软锰矿:MnO2含量≥65%,SiO2含量约20%,Al2O3含量约4%,其余为水分;闪锌矿:ZnS含量≥80%,FeS、CuS、SiO2含量约7%,其余为水分。科研人员开发了综合利用这两种资源的同槽酸浸工艺,工艺流程如以下图所示。
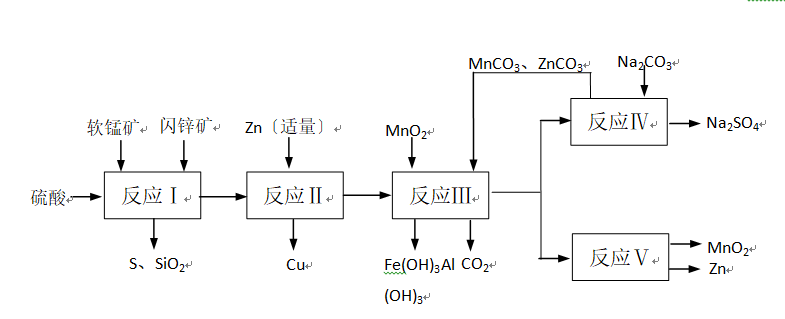
请答复以下问题:
问题一、反应Ⅰ后过滤所得滤液中含有MnSO4、ZnSO4、CuSO4、Fe2(SO4)3、Al2(SO4)3等。试写出反应Ⅰ中生成CuSO4的化学方程式()。
问题二、反应Ⅱ加入适量锌的作用是()。如果锌过量,还会进一步发生反应的离子方程式为()。
问题三、反应Ⅴ的条件是电解,电解时均用惰性电极,阳极发生的电极反应可表示为()。
问题四、本工艺所用的原料除软锰矿、闪锌矿、硫酸外还需要()等原料。
第8题
A.可能含CuSO4和Na2CO3
B.一定含NaCl,可能含Ba(NO3)2、Na2SO4,一定不含Na2CO3、CuSO4
C.一定含NaCl、Ba(NO3)2、Na2SO4,一定不含Na2CO3,可能含CuSO4
D.可能含NaCl,一定含Ba(NO3)2、Na2SO4,一定不含Na2CO3、CuSO4
第9题
A、Cu(OH)2↓+H2S↑+Na2SO4
B、CuS↓+Na2SO4
C、Cu↓+S↓+Na2SO4
D、以上答案都不对
第10题
| 硫酸铜是精炼铜的主要原料,某工厂用硫化铜(CuS)制硫酸铜,拟选择两个方案。 方案①:CuS在硫杆菌(催化剂)的作用下跟空气中的O2反应生成CuSO4 方案②: (1)请写出方案①反应的化学方程式:____________________________________________; (2)从环境保护的角度考虑,上述方案应选___________(填“①“②”)更合理,理由是_____________________________________________________________________。 |
第11题
A.H2S通入CuSO4溶液中:H2S+Cu2+==CuS↓+2H+
B.lCl3溶液与Na2S溶液混合生成沉淀::2 Al3++3S2-==Al2S3↓
C.用惰性电极电解BaCl2溶液:2Cl-+2H2O Cl2↑+H2↑+2OH-
D.用TiCl4制备TiO2的第一步反应:Ti4++ (x+2) H2O(过量) TiO2•xH2O↓+ 4H+

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
