 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
 更多“将40mL0.10mol·L-1AgNO3溶液与10mL0.15mol·L-1NaBr溶液混合,计算溶液中Ag+和Br-的浓度。”相关的问题
更多“将40mL0.10mol·L-1AgNO3溶液与10mL0.15mol·L-1NaBr溶液混合,计算溶液中Ag+和Br-的浓度。”相关的问题
第1题
第2题
将20 cm30.025 mol.dm-3的AgNO3溶液与2.0 cm31.0mol.dm-3的氨溶液混合,所得溶液中Ag(NH3)2+浓度是多少?在此溶液中再加入2.0 cm31.0mol.dm-3的KCN,求所得溶液中Ag(NH3)2+浓度是多少(忽略CN-水解)?配位反应的方向与配合物稳定性关系如何?
第3题
将10.0mL0.10mol·L-1AgNO3溶液与10.0mL1.0mol·L-1氨水混合,计算反应达平衡时Ag+的浓度;若以10.0mL1.0mol·L-1NaCN溶液代替氨水,平衡后溶液Ag+的浓度又是多少?已知Ks([Ag(NH3)2]+)=1.1×107,Ks([Ag(CN)2]-)=1.3×1021。
第4题
等体积混合0.30mol·L-1NH3溶液、0.30mol·L-1NaCN溶液和0.030mol·L-1AgNO3溶液,求平衡时[Ag(CN)2]-和[Ag(NH3)2]+的浓度。已知Kf([Ag(CN)2]-)=1.26×1021,Kf([Ag(NH3)2]+)=1.6×107。
第5题
将3.0dm30.20mol·dm3K[Ag(CN)2]溶液和2.0dm30.30mol·dm-3KI溶液混合,是否会产生AgI沉淀?如欲不产生AgI沉淀,需先在K[Ag(CN)2]溶液中至少加入多少摩尔固体KCN(忽略体积变化)。已知K稳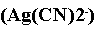 =1.3×1021,Ksp(AgI)=8.3×10-17。
=1.3×1021,Ksp(AgI)=8.3×10-17。
第6题
将一块纯铜片置于0.050mol/L AgNO3溶液中,计算溶液达到平衡后的组成。已知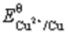 (Cu2+/Cu)=0.337V,
(Cu2+/Cu)=0.337V,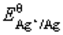 (Ag+/Ag)=0.80V。(提示:首先计算出反应平衡常数。)
(Ag+/Ag)=0.80V。(提示:首先计算出反应平衡常数。)
第7题
0 cm30.20 mol.dm-3的HCl溶液与10.0 cm30.50 mol.dm-3的NaAc溶液混合后,计算: (1)溶液的pH是多少? (2)在混合溶液中加入1.0 cm30.50 mol.dm-3的NaOH,溶液的pH变为多少? (3)在混合溶液中加入1.0 cm30.50 mol.dm-3的HCl,溶液的pH变为多少? (4)将最初的混合溶液用水稀释一倍,溶液的pH又是多少? 以上计算结果说明什么问题?
第8题
第9题
将50mL0.020mol.L—1MgCl2溶液与150mL1.0mol.L—1NH3.H2O溶液混合,通过计算说明: (1)能否产生Mg(OH)2沉淀。 (2)若先在MgCl2溶液中加入100mL1.0mol.L—1 HCl溶液后再与NH3.H2O溶液混合,能否产生Mg(OH)2沉淀? {KspΘ[Mg(OH)2]=5.1×10—12,KspΘ(NH3)=1.76×10—5)
第10题
将生理盐水和50g/L的葡萄糖溶液等体积混合,通过计算说明此混合液是等渗溶液、还是高渗溶液或低渗溶液?
第11题

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
