 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
理想气体A、B和C的热力学数据如下:
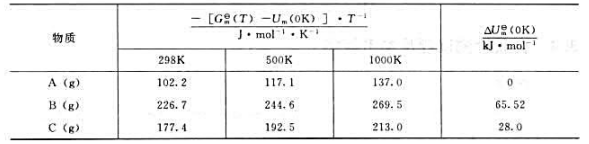
试计算2C(g)=A(g)+B(g)在298K.500K和1000K时反应的标准平衡常数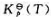 .
.
 更多“理想气体A、B和C的热力学数据如下:试计算2C(g)=A(g)+B(g)在298K.500K和1000K时反应的标准平衡”相关的问题
更多“理想气体A、B和C的热力学数据如下:试计算2C(g)=A(g)+B(g)在298K.500K和1000K时反应的标准平衡”相关的问题
第1题
查表列出298K时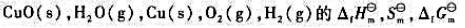 等热力学数据,试据此计算下列反应298K时的
等热力学数据,试据此计算下列反应298K时的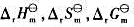 和1000K时的
和1000K时的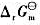 ,并进一步讨论反应的逆转温度。
,并进一步讨论反应的逆转温度。
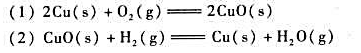
第2题
化学反应如下:CH3COOH(g)-CH4+CO2(g),298.15K各物质的数据为

求上述反应在1000K时的标准摩尔反应焓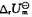 和标准摩尔反应热力学能
和标准摩尔反应热力学能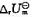 。
。
第3题
已知反应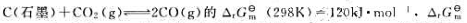 (1000K)=-3.4kJ·mol-1,计算(1) 在标准状态及温度分别为298K和1000K时的标准平衡常数;(2)当1000K时,p(CO)=200kPa,p(CO2)=800kPa,判断该反应方向。
(1000K)=-3.4kJ·mol-1,计算(1) 在标准状态及温度分别为298K和1000K时的标准平衡常数;(2)当1000K时,p(CO)=200kPa,p(CO2)=800kPa,判断该反应方向。
第4题
第5题
制备半导体材料时发生如下反应,其相应的热力学数据如下: SiO2(s)+2C(s)===Si(s)+2CO(g) △fmθ(298.15 K)/(kJ.mol-1) 一903.5 0 0 一110.5 △fGmθ(298.15 K)/(kJ.mol-1) 一850.7 0 0 —1 37.2 试通过计算回答:(1)标准状态下,298.15 K时,反应能否自发进行? (2)标准状态下,反应自发进行的温度条件如何?
第6题
根据表中给出的298K时的热力学数据:

试求算下面反应:

298K时的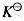 和该温度下固体表面平衡水汽分压。
和该温度下固体表面平衡水汽分压。
第7题
已知下列100kPa,298K时的热力学数据:
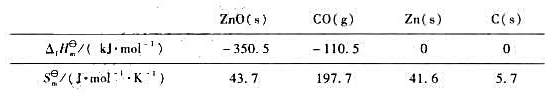
(1)试通过热力学计算,说明下面反应298K时的进行方向:
ZnO(s)+C(s)=Zn(s)+CO(g)
(2)求算上面反应自发正向进行的最低温度。
第8题
已知下列可逆反应: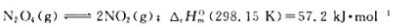 利用有关物质的热力学数据,计算此可逆反应在298.15K和350.15K时的标准平衡常数。
利用有关物质的热力学数据,计算此可逆反应在298.15K和350.15K时的标准平衡常数。
第10题
试根据下列数据求算反应:C2H4(g)+H2(g)=C2H6(g),在1000K时的标准平衡常数Kθ。已知:
(1)在298K时,乙烯和乙烷的标准燃烧热分别为-1411和-1560kJ·mol-1,液态水的标准生成热为-286kJ·mol-1;
(2)在298K时,C2H4(g) 、C2H6(g)和H2(g)的标准熵分别为219. 5、229.5和130.6J·K-1·mol-1;
(3)在298K~1000K范围内,反应的平均热容差△Cp=10.8J·K-1·mol-1。
第11题
反应 在氢能源的利用中具有重要的意义。根据下面的热力学数据计算1000K、标准状态下,每克氢气最多可做多少非体积功?
在氢能源的利用中具有重要的意义。根据下面的热力学数据计算1000K、标准状态下,每克氢气最多可做多少非体积功?


 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
