 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
在298K,将一个铜电极浸在一种含有1.00mo1·L-1氨和1.00mol·L-1[Cu(NH3)4]2+的溶液中,用标准氢电极作正极,测得它和铜电极之间的电势差为0.030V。试计算[Cu(NH3)4]2+的稳定常数。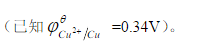
 更多“在298K,将一个铜电极浸在一种含有1.00mo1·L-1氨和1.00mol·L-1[Cu(NH3)4]2+的溶液中,用标准氢电极作正”相关的问题
更多“在298K,将一个铜电极浸在一种含有1.00mo1·L-1氨和1.00mol·L-1[Cu(NH3)4]2+的溶液中,用标准氢电极作正”相关的问题
第1题
将铜电极浸在含有1.00mol·dm-3氨和1.00mol·dm-3[Cu(NH3)4]2+溶液里,以标准锌电极为负极,测得电池的电动势为0.712V。试计算[Cu(NH3)4]2+的稳定常数。
第2题
将一块铜板浸在NH3.H2O和[Cu(NH3)。4]2+的混合溶液中,组成一
![将一块铜板浸在NH3.H2O和[Cu(NH3)。4]2+的混合溶液中,组成一电极,其中NH3和的平衡](https://img2.soutiyun.com/ask/uploadfile/9144001-9147000/bb7ffc43f07b0ae404f872ee951eb7d5.jpg) 电极,其中NH3和
电极,其中NH3和
![将一块铜板浸在NH3.H2O和[Cu(NH3)。4]2+的混合溶液中,组成一电极,其中NH3和的平衡](https://img2.soutiyun.com/ask/uploadfile/9144001-9147000/1b60136accccf00340e054aefa98983d.jpg) 的平衡浓度皆为1.0 mol.dm-3,若用标准氢电极做正极,与上述铜一铜氨配离子电极组成一个原电池,测得该电池的电动势为
的平衡浓度皆为1.0 mol.dm-3,若用标准氢电极做正极,与上述铜一铜氨配离子电极组成一个原电池,测得该电池的电动势为
![将一块铜板浸在NH3.H2O和[Cu(NH3)。4]2+的混合溶液中,组成一电极,其中NH3和的平衡](https://img2.soutiyun.com/ask/uploadfile/9144001-9147000/4f346abe9b967b001a4fcf92ea73bbf0.jpg) ,试根据此计算铜氨配离子
,试根据此计算铜氨配离子
![将一块铜板浸在NH3.H2O和[Cu(NH3)。4]2+的混合溶液中,组成一电极,其中NH3和的平衡](https://img2.soutiyun.com/ask/uploadfile/9144001-9147000/65a9e2521fbf5569d37c3c2697508572.jpg) 的不稳定常数K不稳。[
的不稳定常数K不稳。[
![将一块铜板浸在NH3.H2O和[Cu(NH3)。4]2+的混合溶液中,组成一电极,其中NH3和的平衡](https://img2.soutiyun.com/ask/uploadfile/9144001-9147000/3ca109342a8a572f3775411b80053798.jpg) (Cu2+/Cu)=0.34 V]
(Cu2+/Cu)=0.34 V]
第4题
第5题
第6题
A.大于-0.06V
B.等于-0.06V
C.小于-0.06V
D.不能判定
第7题
A.大于-0.06V
B.-0.06V
C.小于-0.06V
D.不能判定
第8题
在298K时,用铜电极电解铜氨溶液,已知溶液中每1000g水中含CuSO4;15.96g、NH317.0g,当有0.01mol电子的电荷量通过以后,在103.66g阳极部溶液中含有2.091gCuSO4、1.571gNH3。试求:

第9题
A.大于-0.06V
B.等于-0.06V
C.小于-0.06V
D.不能判定

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
