 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
A.1.39V
B.0.62V
C.0.92V
D.1.07V
 更多“已知25℃时,EΘ(Fe3+/Fe2+)=0.77V,EΘ(Sn4+/Sn2+)=0.15V。今有一电池,其电池反应为2 Fe3++Sn2+===Sn4++2Fe2+,则”相关的问题
更多“已知25℃时,EΘ(Fe3+/Fe2+)=0.77V,EΘ(Sn4+/Sn2+)=0.15V。今有一电池,其电池反应为2 Fe3++Sn2+===Sn4++2Fe2+,则”相关的问题
第1题
已知25℃时EΘ(Fe3+/Fe)=-0.036V,EΘ(Fe3+/Fe2+)=0.770V。试计算25℃时电极(Fe2+/Fe)的标准电极电势EΘ(Fe2+/Fe)。
第2题
已知25°C时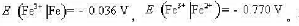 试计算应25°C时电极Fe2+|Fe的标电极电势E(Fe2+|Fe)。
试计算应25°C时电极Fe2+|Fe的标电极电势E(Fe2+|Fe)。
第3题
试计算25℃时,反应Sn+Pb2+===Sn2++Pb的
第4题
已知25℃时AgBr的溶度积Ksp=4.88×10-13,EΘ(Ag+/Ag)=0.7994V,EΘ(Br2/Br-)=1.065V,试计算25℃时:(1)银-溴化银电极的标准电极电势EΘ(AgBr(s)/Ag);(2)AgBr(S)的标准生成吉布斯函数。
第5题
101.3kPa,25℃下,下列反应的反应焓为5.36kJ·mol-1:
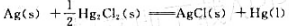
已知25℃时,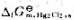 =-210.7kJ·mol-1,
=-210.7kJ·mol-1,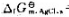 =-109.7kJ·mol-1,请:
=-109.7kJ·mol-1,请:
(1)试为上述反应设计一可逆电池,写出电池表示式和电极反应;
(2)求所设计电池的电动势及其温度系数和电池反应的ΔtGmθ、ΔtSmθ:
(3)求25℃时,电极C1-|Hg2Cl2|Hg的标准电极电位;
已知25℃时,Eθ[Ag+|AgCl(s)|Ag]=0.2224V
(4)已知25℃时Eθ(Hg22+|Hg)=0,798V,求Hg2Cl2在25℃时的溶度积.
第6题
在25℃时,电池
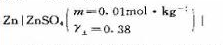
|PbSO4-Pb(s)的电动势E=0.5477V.(1)已知φθ(Zn2+|Zn)=-0.763V,求φθ(PbSO4|Pb(2)已知25℃时PbSO4的K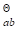 =1.58×10-8,求φθ(Pb2+|Pb);(3)当ZuSO4的m=0.050mol·kg-1时,E=0.5230V,求此浓度下ZnSO4的y
=1.58×10-8,求φθ(Pb2+|Pb);(3)当ZuSO4的m=0.050mol·kg-1时,E=0.5230V,求此浓度下ZnSO4的y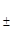 .
.
第8题
25℃时,下列电池的电动势E=1.1365V,电动势的温度系数
Ag|AgCl(s)|HCl(a±=0.6)|Cl2(g,100kPa)|Pt
已知25℃时Ag(s)与Cl2(g)的标准熵分别为42.55J·K-1·mol-1及223.07J·K-1·mol-1。试求AgCl(s)25℃时的
第10题
已知25℃时下列电极的标准电极电势;
①Cu2+ICu(s)Eθ=0.3402V ②Cu+|Cu (s)Eθ=0.5224 V
则电极Cu2+,Cu+|Pt(s)的标准电极电势Eθ(Cu2+,Cu+)=().

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
