 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
已知反应:C2H5Br(g)→C2H4(g)+HBr(g),其活化能是226kJ·mol-1,650K时,速率常数为2.0×10-5s-1,试计算在哪个温度时速率常数是6.0×10-5s-1?
 更多“已知反应:C2H5Br(g)→C2H4(g)+HBr(g),其活化能是226kJ·mol-1,650K时,速率常数为2.0×10-5s-1,试计算在哪个温”相关的问题
更多“已知反应:C2H5Br(g)→C2H4(g)+HBr(g),其活化能是226kJ·mol-1,650K时,速率常数为2.0×10-5s-1,试计算在哪个温”相关的问题
第1题
第2题
A.-44.2kJ·mol-1
B.+44.2kJ·mol-1
C.-330kJ·mol-1
D.+330kJ·mol-1
第3题
试根据下列数据求算反应:C2H4(g)+H2(g)=C2H6(g),在1000K时的标准平衡常数Kθ。已知:
(1)在298K时,乙烯和乙烷的标准燃烧热分别为-1411和-1560kJ·mol-1,液态水的标准生成热为-286kJ·mol-1;
(2)在298K时,C2H4(g) 、C2H6(g)和H2(g)的标准熵分别为219. 5、229.5和130.6J·K-1·mol-1;
(3)在298K~1000K范围内,反应的平均热容差△Cp=10.8J·K-1·mol-1。
第4题
已知乙烯氧化制环氧乙烷,可发生下列两个反应:
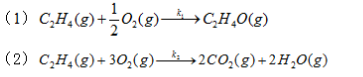
在298K时物质的标准摩尔生成Gibbs自由能数据如下:
| 物质 | C2H4O(g) | C2H4(g) | CO2(g) | H2O(g) |
| Delta _fG_m^{ominus }/(kJcdot mol^{-1}) | -13.1 | 68.1 | -394.4 | -228.6 |
当在银催化剂上,研究上述反应时得到反应(1)及反应(2)的反应级数完全相同,E1=63.6kJ·mol-1,E2=82.8kJ·mol-1,而且可以控制C2H4O(g)进一步氧化的速率极低。
第6题
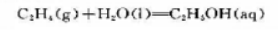
已知25℃纯乙醇的蒸气压为7.60×102Pa,乙醇水溶液在其标准态(即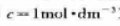 )时,乙醇的蒸气压为5.33×102Pa,C2H5OH(l)、H2O(l)和C2H4(g)的标准生成吉布斯自由能分别为-1.748×105、-2.372×105和6.818×104J.mol-1.试求算此水合反应的标准平衡常数.
)时,乙醇的蒸气压为5.33×102Pa,C2H5OH(l)、H2O(l)和C2H4(g)的标准生成吉布斯自由能分别为-1.748×105、-2.372×105和6.818×104J.mol-1.试求算此水合反应的标准平衡常数.
第7题

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
