 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
已知电极反应 (Ag+/Ag)=0.7991V,Ag2C2O4的溶度积为3.4×10-11,计算电极反应
(Ag+/Ag)=0.7991V,Ag2C2O4的溶度积为3.4×10-11,计算电极反应 的标准电极电势
的标准电极电势
 更多“已知电极反应(Ag+/Ag)=0.7991V,Ag2C2O4的溶度积为3.4×10-11,计算电极反应的标准电极电势(Ag2C2O4/Ag)。”相关的问题
更多“已知电极反应(Ag+/Ag)=0.7991V,Ag2C2O4的溶度积为3.4×10-11,计算电极反应的标准电极电势(Ag2C2O4/Ag)。”相关的问题
第1题
A.0.799
B.0.2
C.0.675
D.0
第2题
第3题
第4题
第5题
第6题
A.0.799
B.0.360
C.0.675
D.0
第7题
第8题
已知Eθ(Ag+/Ag)=+0.799 V,Kspθ(AgCl)=1.56×10-10。若在半电池Ag|Ag+(1 mol.L-1)中加入KCl,使其变成Ag,AgCl|KCl(1 mol.L-1),则其电极电势将 ()
A.增加0.220 V
B.降低0.220 V
C.增加0.581 V
D.降低0.581 V
第9题
已知E(Ag+/Ag)=0.7996V,Ksp(Ag2CrO4)=1.12×10-12,计算电极反应
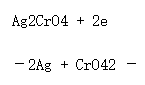 的标准电极电势以及当
的标准电极电势以及当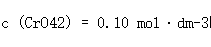 时该电极反应的电势值。
时该电极反应的电势值。
第10题
10.已知

的标准电极电势以及当

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
