 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
已知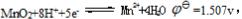 Fe3++e-===Fe2+EΘ=0.771V
Fe3++e-===Fe2+EΘ=0.771V
(1)判断下列反应的方向,并配平
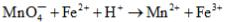
(2)将这两个半电池组成原电池,用电池符号表示该原电池的组成,标明电池的正、负极,并计算其标准电动势。
(3)当氢离子浓度为10mol·L-1,其他各离子浓度均为1mol·L-1时,计算该电池的电动势。
 更多“已知 Fe3++e-===Fe2+ EΘ=0.771V (1)判断下列反应的方向 (2)将这两个半电池组成原电池,用电池符号”相关的问题
更多“已知 Fe3++e-===Fe2+ EΘ=0.771V (1)判断下列反应的方向 (2)将这两个半电池组成原电池,用电池符号”相关的问题
第1题
A.c(Fe3+)<1
B.c(Fe2+)<1
C.c(Fe2+/c(Fe3+)<1
D.c(Fe3+)/c(Fe2+)<1
第2题
已知:Fe3++e-=Fe2+,EΘ=0.771V;
[Fe(CN)6]3-+e-=[Fe(CN)6]4-,EΘ=0.358V;
Fe3++6CN-⇌[Fe(CN)6]3-,K稳=1.00x10^42。
求反应Fe2++6CN-⇌[Fe(CN)6]4-的![已知:Fe3++e-=Fe2+,EΘ=0.771V;[Fe(CN)6]3-+e-=[Fe(CN)6]](https://img2.soutiyun.com/ask/2020-06-08/960457706742811.png) 。
。
第3题
已知:Fe3++e-=Fe2+,EAθ=0.77V。Fe(OH)3的Kspθ=2.8x10^-9,Fe(OH)2的Kspθ=4.9x10^-17。求半反应Fe(OH)3+e-=Fe(OH)2+OH-的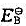 。
。
第4题
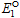 =-0.439V (2)Fe3++e-====Fe2+的标准电极电势
=-0.439V (2)Fe3++e-====Fe2+的标准电极电势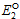 =0.770V (3)Fe3++3e-====Fe(s)所对应电极的标准电极电势
=0.770V (3)Fe3++3e-====Fe(s)所对应电极的标准电极电势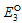 {Fe3+|Fe(s)}=( )。
{Fe3+|Fe(s)}=( )。A.0.331V
B.-0.036V
C.-0.331V
D.0.036V
第6题
第9题
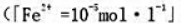
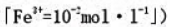 时Fe3++e-=Fe2+的电极电势,由此估算指示剂的标准电极电势应为多大。
时Fe3++e-=Fe2+的电极电势,由此估算指示剂的标准电极电势应为多大。
第10题
已知25℃时EΘ(Fe3+/Fe)=-0.036V,EΘ(Fe3+/Fe2+)=0.770V。试计算25℃时电极(Fe2+/Fe)的标准电极电势EΘ(Fe2+/Fe)。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
