 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
已知Hg-T1二组分系统的数据如下:
物质 Hg Tl2Hg6Tl 最低共熔点E1最低共熔点E2 w(Tl)=8% w(Tl)=41% |
| 熔点/℃ -39 15 303 -60 0.4 |
 更多“已知Hg-T1二组分系统的数据如下: 物质 Hg Tl2Hg6 Tl 最低共熔点E1 最低共”相关的问题
更多“已知Hg-T1二组分系统的数据如下: 物质 Hg Tl2Hg6 Tl 最低共熔点E1 最低共”相关的问题
第1题
已知Hg-TI二组分系统的数据如下:
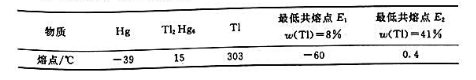
(1)绘制其温度一组成图(示意图);
(2)指出各相区,水平线段、交点的相数;
(3)为扩大低温测量范围,应选什么组成的Hg-TI混合物做温度计较合适?
第2题
已知A、B二组分系统的相图如下:
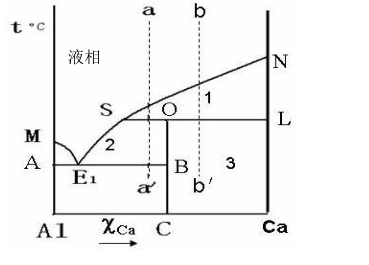
(1)标出数字所标相区的相态,指出自由度为零的地方
(2)画出a、b两个系统冷却时的步冷曲线
(3)指出水平线上有哪几相平衡共存
第4题
对FeO-MnO二组分系统,已知FeO和MnO的熔点分别为1370℃和1785℃,在1430℃,分别含有40%和70%的FeO(质量分数)的二固体溶液相发生转熔变化,其平衡的液相组成为85%的FeO。在1200℃时,二固溶体的组成为36%的FeO和74%的MnO,试依据上述数据:

第5题
乙醇(1)-甲苯(2)系统的有关的平衡数据如下:T=318K,p=24.4kPa,x1=0.300,y1=0.634,已知318K的两组饱和蒸气压为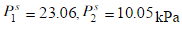 ,并测得液相的混合热是一个仅与温度有关的常数△H/RT=0.437,令气相是理想气体,求(a)液相各组分的活度系数;(b)液相的△G和GE;(c)估计333K,x1=0.300时的GE值;(d)由以上数据能否计算出333K,x1=0.300时液相的活度系数?为什么?(e)该溶液是正偏差还是负偏差?
,并测得液相的混合热是一个仅与温度有关的常数△H/RT=0.437,令气相是理想气体,求(a)液相各组分的活度系数;(b)液相的△G和GE;(c)估计333K,x1=0.300时的GE值;(d)由以上数据能否计算出333K,x1=0.300时液相的活度系数?为什么?(e)该溶液是正偏差还是负偏差?
第6题
电解熔融的LiCl(s)制备金属Li(s)时。常常要加一定量的KCl(s) ,这样可以节约能源。已知LiCl(s)的熔点为878 K,KCl(s)的熔点为1 048K,LiCI(A)与KCI(B)组成的二组分系统的低共熔点为629 K,这时KCl(B)的质量分数wg=0.50.在723 K时KCl(B)含量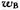 =0.43的熔化物冷却时,首先析出LiCl(s),而
=0.43的熔化物冷却时,首先析出LiCl(s),而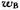 =0.63的熔化物冷却时首先析出KCl(s)。
=0.63的熔化物冷却时首先析出KCl(s)。
(1)画出LiCl(A)与KCl(B)的二组分系统的低共熔相图;
(2)简述加一定量KCl(s)的原因;
(3)电解槽操作温度应高于哪个温度,为什么?
(4)KCl(s)加入的质量分数应控制在哪个范围内为好?
第7题
Zn(A)和Mg(B)形成的二组分低共熔相图具有两个低共熔点,一个含Mg的质量分数为0.032 ,温度为641 K;另一个含Mg的质量分数为0.49,温度为620 K.在系统的熔液组成曲线上有一个最高点,含Mg的质量分数为0.157,温度为863K.已知Zn(s)和Mg(s)的熔点分别为692K和924K. (1)试画出Zn(A)和Mg(B)形成的二组分低共熔相图,并分析各区的相态和自由度;(2)分别用相律说明,含Mg的质量分数为0.80和0.30熔化物从973 K冷却到573 K过程中的相变和自由度变化;(3)分别画出含Mg的质量分数为0.80、0.49和0.30熔化物,从973K冷却到573K过程中的步冷曲线。
第9题
Zn(A)和Mg(B)形成的二组分低共熔相图具有两个低共熔点,一个含Mg的质量分数为0.032,温度为641K;另一个含Mg的质量分数为0.49,温度为620K。在系统的熔液组成曲线上有一个最高点,含Mg的质量分数为0.157,温度为863K。已知Zn(s)和Mg(s)的熔点分别为692K和924K。(1)试画出Za(A)和Mg(B)形成的二组分低共熔相图,并分析各区的相态和自由度;(2)分别用相律说明,含Mg的质量分数为0.80和0.30熔化物从973K冷却到573K过程中的相变和自由度变化;(3)分别画出含Mg的质量分数为0.80、0.49和0.30熔化物,从973K冷却到573K过程中的步冷曲线。
第10题
已知理想气体反应SO2(g)+½SO2(g)→SO2(R)的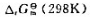 =270kJ·mol-1,25℃下各反应组分的吉布斯自由能函数数据如下:
=270kJ·mol-1,25℃下各反应组分的吉布斯自由能函数数据如下:
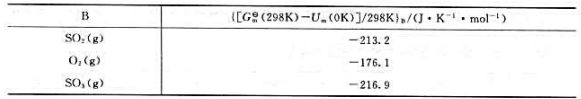
计算此反应的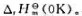

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
