 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
计算pH=5.0时,0.10mol/L H2C2O4溶液中的浓度。(已知:H2C2O4的Ka1=5.9×10-2,Ka2=6.4×10-5)
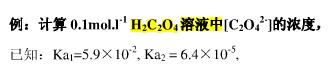
 更多“计算pH=5.0时,0.10mol/L H2C2O4溶液中的浓度。(已知:H2C2O4的Ka1=5.9×10-2,Ka2=6.4×10-5)”相关的问题
更多“计算pH=5.0时,0.10mol/L H2C2O4溶液中的浓度。(已知:H2C2O4的Ka1=5.9×10-2,Ka2=6.4×10-5)”相关的问题
第1题
在pH=5.0和pH=5.5的六亚甲基四胺介质中,以二甲酚橙(XO)为指示剂,分别以0.020mol·L-1EDTA滴定0.020mol·L-1Zn2+和0.10mol·L-1Ca2+混合溶液中的Zn2+,计算上述两种情况下的终点误差各为多少?(lgKZnY=16.5,lgKCaY=10.7;pH=5.0时,lgαY(H)=6.45,pZnep(XO)=4.8;pH=5.5时,lgαY(H)=5.5,pZnep(XO)=5.7;已知XO不与Ca2+发生显色反应)
第2题
计算pH=5.0时Co2+和EDTA配合物的条件稳定常数(不考虑水解等副反应)。当Co2+抖浓度为0.02mol/L时,能否用EDTA准确滴定?
第3题
第4题
(1)计算pH=5.0时,H3PO4的分布系数δ3、δ2、δ1、δ0。(2)假定H3PO4各种形式的总浓度是0.050mol/L,问此时H3PO4,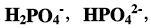
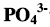 的浓度各为多少?
的浓度各为多少?
第8题
用0.10mol/L NaOH滴定0.10mol/L HAc至pH=8.00,计算终点误差。[Ka(HAc)=1.8×10-5]
第9题

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
