 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
试计算,在Cu-Zn电池中当


 更多“试计算,在Cu-Zn电池中当的比值为多大时,电池才停止工作?已知=-0.7628V,=0.337V。”相关的问题
更多“试计算,在Cu-Zn电池中当的比值为多大时,电池才停止工作?已知=-0.7628V,=0.337V。”相关的问题
第1题
第2题
当下列电池中的溶液是H=4.00时的缓冲溶液时,在25℃测得电池的电动势为0.209V。
(—)玻璃电极|H+(a=x) 当缓冲溶液由未知溶液代替时,测得电池电动势如下: (1)0.312V; (2)0.098V;(3)=0.017V。试计算每种溶液的pH值。
当缓冲溶液由未知溶液代替时,测得电池电动势如下: (1)0.312V; (2)0.098V;(3)=0.017V。试计算每种溶液的pH值。
第3题
当下列电池中的溶液是pH=4.00的缓冲溶液时,在25℃测得电池的电动势为0.209V:玻璃电极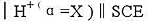 当缓冲溶液由未知溶液代替时,测得电池电动势如下:
当缓冲溶液由未知溶液代替时,测得电池电动势如下:
(a)0.312V; (b)0.088V; (c)-0.017V.试计算每种溶液的pH.
第4题
第5题
第6题
A.盐桥中的电解质可保持两个半电池中的电荷平衡
B.盐桥为原电池构成一个闭合回路,使两电极反应能继续进行
C.盐桥中的电解质不能参与电池反应
D.电子通过盐桥流动
第7题
A.盐桥中的电解质可保持两个半电池中的电荷平衡
B.盐桥为原电池构成一个闭合回路,使两电极反应能继续进行
C.盐桥中的电解质不能参与电池反应
D.电子通过盐桥流动
第8题
第9题
298K时测定下述电池的电动势:
玻璃电极|pH缓冲溶液|饱和甘汞电极
当所用缓冲溶液的pH=4.00时,测得电池的电动势为0.1120V。若换用另一缓冲溶液重测电动势,得E=0.3865V。试求该缓冲溶液的pH值。当电池中换用pH=2.50的缓冲溶液时,计算电池的电动势E。
第10题
当下列电池中的标准溶液是pH=5.21的缓冲溶液时,在25℃时的电动势为0.209V。
玻璃电极|H+(a)||SCE。
当缓冲溶液由待测试液代替时,测得的电动势为0.312V,计算待测试液的pH。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
