 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
 更多“称取含有NaCl和NaBr的试样0.5776g,用重量法测定,得到二者的银盐沉淀为0.4403g;另取同样质量的试样,用沉淀滴定法滴定,消耗0.1074mol·L-1AgNO325.25mL溶液.求N…”相关的问题
更多“称取含有NaCl和NaBr的试样0.5776g,用重量法测定,得到二者的银盐沉淀为0.4403g;另取同样质量的试样,用沉淀滴定法滴定,消耗0.1074mol·L-1AgNO325.25mL溶液.求N…”相关的问题
第1题
称取含有NaCl和NaBr的试样0.6280g,溶解后用AgNO3溶液处理,得到干燥的AgCl和AgBr沉淀0.5064g。另称取相同质量的试样1份,用0.1050mol/L AgNO3溶液滴定至终点,消耗28.34mL。计算试样中NaCl和NaBr的质量分数。
第2题
称取含有NaCl和NaBr的样式0.6280g,溶解后用AgNO3溶液处理,得到干燥的AgCl和AgBr沉淀0.5064g。另称取相同质量的试样一份,用0.1050mol·L-1AgNO3溶液滴定至终点,消耗28.34mL。计算试样中NaBr和NaCl的质量分数。
第3题
称取含NaCl和NaBr的试样0.5000g,溶解后用0.1000mol·L-1AgNO3溶液滴定,终点时耗去22.00mL。另取0.5000g试样,溶解后用AgNO3处理得到沉淀质量为0.4020g。计算试样中NaCl、NaBr的质量分数。[M(NaCl)=58.44g·mol-1,M(NaBr)=102.9g·mol-1,M(AgCl)=143.3g·mol-1,M(AgBr)=187.8g·mol-1]
第4题
含硫约36%的黄铁矿,用沉淀重量法测定硫,欲得0.50g左右的BaSO4沉淀,问应称取试样若干克?
第5题
用KMnO4法测定硅酸盐试样中的Ca2+含量。称取试样0.5863g,在一定条件下,将钙沉淀为CaC2O4,过滤、洗涤沉淀。将洗净的CaC2O4溶解于稀H2SO4中,用0.05052mol·L-1KMnO4标准溶液滴定,消耗25.64mL。计算硅酸盐中Ca的质量分数。
第7题
用KMnO4法测定硅酸盐样品中Ca2+的含量,称取试样0.5863g,在一定条件下,将钙沉淀为CaC2O4,过滤、洗涤沉淀,将洗净的CaC2O4溶于稀H2SO4中,用c(KMnO4)=0.05052mol/L的KMnO4标准滴定溶液滴定,消耗25.60mL,计算硅酸盐中Ca的质量分数。
第8题
重量分析法用于测定矿石中的磁铁矿(Fe3O4)的含量。称取1.5419g试样,用浓盐酸溶解后,得到Fe2+和Fe3+的混合溶液。加入硝酸将Fe2+氧化至Fe3+,稀释后用氨水将Fe3+沉淀为Fe(OH)3。将沉淀过滤,洗涤和灼烧后得0.8525gFe2O3,计算Fe2O3的质量分数?已知摩尔质量:Fe2O3为159.69g·mol-1Fe3O4为231.55g·mol-1.
第9题
称取含铝试样0.5000g,溶解后用8-羟基喹啉沉淀,得到0.3200gAl(C9H6NO)3沉淀。计算试样中铝的质量分数。沉淀形式若为Al2O3,可得到多少克Al2O3沉淀物?[M(Al)=26.98g·mol-1,M(AlC27H18N3O3)=459.44g·mol-1,们(Al2O3)=101.96g·mol-1]
第10题
已知某试样可能含有Na3PO4,Na3HPO4和惰性物质。称取该试样1.0000g,用水溶解。试样溶液以甲基橙作指示剂,用0.2500mol·L-1HCl溶液滴定,用去了32.00mL。含同样质量的试样溶液以百里酚酞作指示剂,需上述HCl溶液12.00mL。求试样中Na3PO4和Na2HPO4的质量分数。
第11题
用重量法测定试剂Na2HPO4·12H2O的纯度,首先是将试剂中的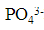 转化为MgNH4PO4·6H2O沉淀,然后灼烧成Mg2P2O7,为了使灼烧后所得的Mg2P2O7的称量误差小于0.1%,问至少应称取多少克试样?(已知相对分子质量:Na2HPO4·12H2O为358.1,MgP2O7为22.6,MgNH2PO4·6H2O为245.9)
转化为MgNH4PO4·6H2O沉淀,然后灼烧成Mg2P2O7,为了使灼烧后所得的Mg2P2O7的称量误差小于0.1%,问至少应称取多少克试样?(已知相对分子质量:Na2HPO4·12H2O为358.1,MgP2O7为22.6,MgNH2PO4·6H2O为245.9)

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
