 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
 更多“下述三种配合物:(1)[Fe(H2O)6]3+,(2)[Co(NH3)6]3-,(3)[Co(NH3)6]2+,试写出它们的d电子排布式,计算它们的磁矩值。”相关的问题
更多“下述三种配合物:(1)[Fe(H2O)6]3+,(2)[Co(NH3)6]3-,(3)[Co(NH3)6]2+,试写出它们的d电子排布式,计算它们的磁矩值。”相关的问题
第1题
已知下列配合物的分裂能(△。)和中心离子的电子成对能(P),写出各中心离子的d电子排布式,并估算它们的磁矩各为多少。指出这些配合物中何者为高自旋型,何者为低自旋型?
配离子 (1)[Co(NH3)6]2+(2) [Fe(H2O)6]2+(3)[Co(NH3)6]3+
P/cm-122500 17600 21000
△。/cm-111000 1040O 22900
第2题
有配合物[Fe(H2O)6]3+、[Co(NH3)6]3+及[Co(NH3)6]2+,试比较它们的△o与P值,写出它们的d电子分布式,估算它们的磁矩值。
第3题
K4[Fe(CN)6]为低自旋配合物,[Fe(H2O)6]Cl3是高自旋配合物。 根据晶体场理论分别写出它们的中心离子的电子排布。
第5题
对比配合物[Fe(H4O)6]SO4和K4[Fe(CN)6]: (1)分别说明它们是低自旋还是高自旋配合物; (2)画出它们的中心金属离子的d电子排布; (3)分别计算它们的CFSE。
第7题
试确定下列配合物是内轨型配合物还是外轨型配合物,说明理由,并以它们的电子层结构表示之。
(1)K4[Mn(CN)6]测得磁矩μ=2.00B.M
(2)(NH4)2[FeF5(H2O)]测得磁矩μ=5.78B.M
第8题
和t2g轨道中的分布,并估计它们的磁矩各约为多少(B.M.).指出这些配合物中何者为商自旋排布,何者为低自旋排布.
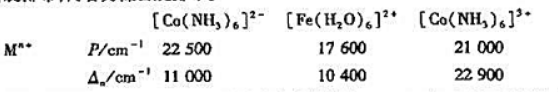
第9题
配位化合物的组成结构和性质,常可用经验规律进行理解,试回答下列问题:
(1)根据十八电子规则,推算下列配合物化学式中的x值:

(2)试计算下列金属膜合物中.金属簇已有的价电子数(g)、金属-金属键的键数(b)及金属簇的几何构型。
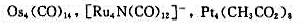
(3)某ML4配合物在低自旋时变成拉长的八面体,试写出配合物中M原子的d电子组态。
(4)对下列配合物:
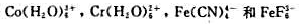
(a)写出它们的d电子组态,哪--种容易出现几何形态的变形效应(即出现了Jahn-Teller效应)?
(b)求出变形的这种配合物的配位场稳定化能(以Δo为单位)。
(c)计算其磁矩(忽略电子的轨道运动对磁矩的贡献)。
第11题
写出O22+、O2+、O2-、O22-的价层电子排布,指出它们键级和磁性,并判断其键能和键长的大小顺序。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
