 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
题目
试证明对遵守范德华(van der waals)方程的实际气体,其恒温可逆膨胀功
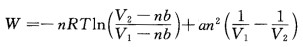 并求0℃时lmol、10dm3的范德华气体恒温可逆膨胀至22.4dm3时的功。已知a=0.14Pa.m6.mol-2,b=3.2×10-5m3.mol-1; (2)若
并求0℃时lmol、10dm3的范德华气体恒温可逆膨胀至22.4dm3时的功。已知a=0.14Pa.m6.mol-2,b=3.2×10-5m3.mol-1; (2)若
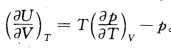 。求范德华气体在恒温可逆膨胀过程中的△U和Q。
。求范德华气体在恒温可逆膨胀过程中的△U和Q。
 更多“试证明对遵守范德华(van der waals)方程的实际气体,其恒温可逆膨胀功 并求0℃时lmol、10dm3”相关的问题
更多“试证明对遵守范德华(van der waals)方程的实际气体,其恒温可逆膨胀功 并求0℃时lmol、10dm3”相关的问题
第2题
(1)试证明对遵守范德华方程的Imal实际气体来说,其等温可逆膨胀功可用下式求算:
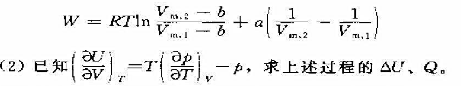
(3)求上述系统在绝热自由膨胀过梐中的温度变化.
第3题
第4题
热膨胀系数的定义为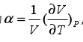 ,试列式表示热膨胀系数与温度、体积的关系。(1)设气体为理想气体;(2)设气体为van der Waals气体。
,试列式表示热膨胀系数与温度、体积的关系。(1)设气体为理想气体;(2)设气体为van der Waals气体。
第5题
第6题
第7题
已知CO2(g)的临界温度、临界压力和临界摩尔体积分别为Tc=304.3K,pc=73.8×105Pa,Vm,c=0.0957dm3·mol-1。(1)试计算CO2(g)的van der Waals常数a、b的值;(2)313K时,在容积为0.005m3的容器内含有0.1kg CO2(g),用van der Waals方程计算气体的压力;(3)在与(2)相同的条件下,用理想气体状态方程计算气体的压力。
第8题
348K时, 0.3kgNH3=3(g)的压力为1.61×103kPa,试用下述两种方法计算其体积。试比较哪种方法计算出来的体积与实测值更接近(已知实测值为28.5dm³)。已知在该条件下NH3(g)的临界参数为Te=405.6K,pc=1.13×104kPa;van der Waals气体常数为a=0.417 Pa·m6·mol-2,b=3.71×10-5m³·mol-1。(1)用van der Waals气体状态方程式;(2)用压缩因子图。
第9题
348K时,0.3kgNH3(g)的压力为1.61×103kPa,试用下述两种方法计算其体积。试比较哪种方法计算出来的体积与实测值更接近(已知实测值为28.5dm3)。已知在该条件下NH3(g)的临界参数为Tc=405.6K,pc=1.13×104kPa;van der Waals气体常数为a=0.417Pa·m6·mol-2,b=3.71×10-5m3·mol-1。(1)用van der Waals气体状态方程式;(2)用压缩因子图。
第10题
一个容积为0.5m3的钢瓶内,放有16kg温度为500K的CH4(g),试计算容器内的压力。(1)用理想气体状态方程;(2)由van der Waals方程。已知CH4(g)的常数a=0.228Pa·m6·mol-2,b=0.427×10-4m3·mol-1,M(CH4)=16.0g·mol。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
